摘要
背景
病毒性呼吸道感染可促進細菌的重複感染,降低宿主的免疫反應效率。然而,我們最近通過一個小鼠模型證明,用細菌提取物OM-85進行預防性治療可以降低繼發性疾病的易感性鏈球菌(年代.)肺炎流感病毒感染後感染。
方法
為了更好地表征OM-85對肺炎鏈球菌進行事後分析,比較OM-85組和對照(BLANC)組小鼠在以下情況下的療效(生存)和發病體征(臨床評分、體溫和體重減輕):a)靜脈感染;b)主肺炎鏈球菌c)靜脈注射後。肺炎鏈球菌超級。
結果
在亞致死的靜脈注射劑量後,所有小鼠在第5天都存活了下來,在OM-85組和BLANC組之間沒有發現疾病體征的差異。然而,OM-85預處理在病毒感染後的第5天顯著降低了肺中的病毒載量,並在第10天減少了中性粒細胞炎症,同時增加了氣道中流感特異性CD8 + t細胞的比例。與病毒感染相反,暴露於肺炎鏈球菌在感染後第3天,BLANC組沒有小鼠存活,而在OM-85預處理小鼠中觀察到部分保護作用(20%的小鼠在第3天存活,第4天和第5天存活10%)。發病率數據證實了生存結果。有趣的是,在“超級感染”研究中,當小鼠暴露在亞致死的靜脈注射劑量下,然後是第二劑量肺炎鏈球菌感染後,BLANC組小鼠在第4天全部死亡。相比之下,OM-85治療組在第4天的生存率為70%,第5天仍然為50%,對臨床評分和第1天和第2天已經檢測到的體溫產生了積極影響。
結論
OM-85預處理對肺炎鏈球菌超級感染反映了來自宿主的強烈而直接的免疫反應,這一事件可以部分解釋為免疫係統的“非特異性”激活,是一般OM-85誘導的免疫反應對靜脈注射的積極“免疫效應”
背景
病毒感染是一般人群致病的主要原因,通常較為輕微,往往局限於上呼吸道[1,2].然而,它們可能發展為下呼吸道感染(RTI)。在這些情況下,可能會發展成嚴重疾病,需要住院治療,並可能導致死亡[3.].越來越多的證據表明,病毒性呼吸道感染可通過降低先天免疫細胞清除細菌的效率來促進細菌的超級感染[4,5],通過破壞氣道上皮表麵,促進細菌粘附,但也抑製適應性免疫反應[6].嚴重的鏈球菌(年代.)肺炎感染加重流感是這一係列事件的經典例子[3.,7,8].增加複發性呼吸道感染易感性的機製總體上反映了宿主防禦效率低下[1,2].出生後,免疫係統成熟並發展出有效控製感染的能力,宿主與環境之間的接觸是進化的絕對必要[9,10].近年來,所謂的“衛生假說”支持了這樣一種觀點:生活在更清潔的環境中不僅會增加過敏和哮喘的風險,還會增加複發性呼吸道感染和其他呼吸道疾病的風險[11,12,13].因此,基於模仿細菌作用的衍生物刺激免疫係統的治療,作為感染的“保護”作用的替代品,已被認為是一種合理的預防方法[14].臨床報告支持這一概念,即接觸細菌成分也可能影響對包括病毒在內的各種其他呼吸道病原體的反應[15,16,17,18,19].在兒童中,使用細菌提取物Broncho Vaxom™(在實驗研究中通常稱為OM-85)治療複發性呼吸道感染是有效的,不僅可以降低複發性呼吸道感染的頻率和持續時間,還可以降低複發性呼吸道感染的強度[16,17,18].此外,OM-85甚至具有抗病毒作用,其機製最近在亞致死流感病毒感染的小鼠模型中得到了表征[20.].在OM-85治療的動物中,肺組織中的病毒載量下降,支氣管肺泡灌洗液中流感特異性CD8+細胞毒性t細胞數量增加。在這些小鼠中,OM-85還導致了樹突狀細胞的非特異性成熟,與抗原呈遞有關的表麵分子過表達。同時,多克隆b細胞活化,血清IgG水平顯著增加,氣道中IgA和IgG有增加趨勢[20.].有趣的是,在“超級感染”的研究中,易感性是次要的肺炎鏈球菌在流感感染後7天誘導的小鼠感染,OM-85可減少感染[20.].OM-85是否對肺炎鏈球菌是否被先前的流感病毒誘導的非特異性免疫反應激活所增強尚不清楚。在一組初步的實驗中,OM-85在保護小鼠免受一種初級肺炎鏈球菌進行了檢測,但沒有報告結果,也沒有與繼發性流感後肺炎鏈球菌研究。對這些初步數據的評價,比較OM-85在以下方麵的活性:a)流感感染;b)主肺炎鏈球菌和c) Post-influenza肺炎鏈球菌超級感染,是本事後分析的目標。
方法
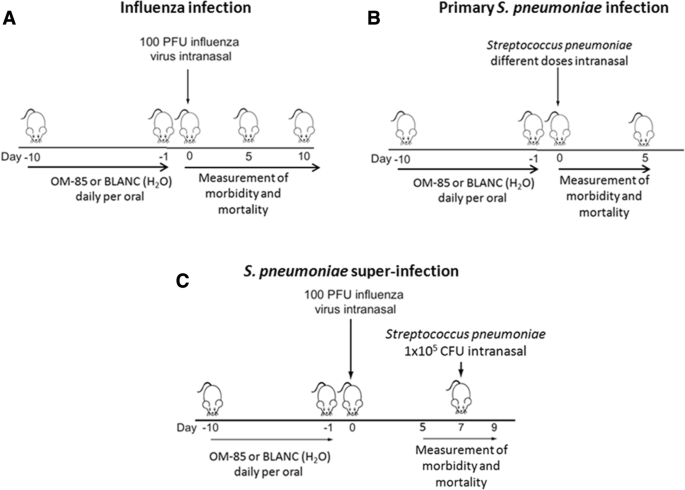
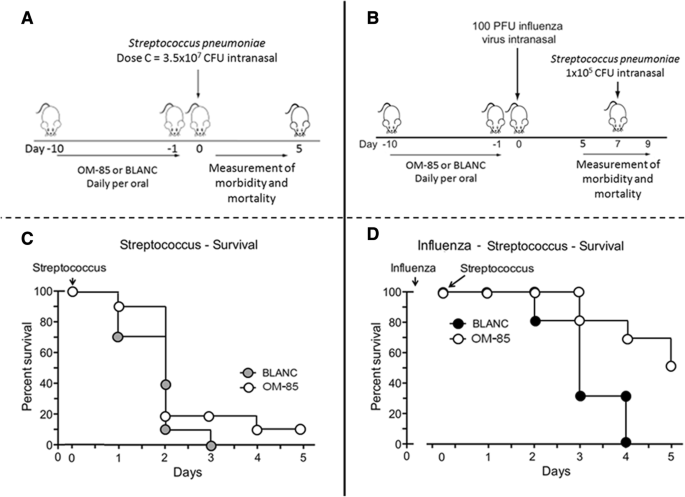
對原始研究設計的詳細描述已在原稿中詳細報道[20.]在此隻作簡要概括。在三項研究中,“流感感染”,“初級肺炎鏈球菌感染”和“肺炎鏈球菌在前10天,8周齡雌性BALB/c小鼠每天灌胃7.2 mg OM-85活性成分,相當於320 μL可溶性OM-85濃縮物,或其等效的不含任何細菌提取物的工程生物過程(簡稱“BLANC”)(圖1)。1a, b和c).8周齡雌性BALB/c小鼠的數量為:A)“流感感染”:每組10隻小鼠至第10天,每組5隻小鼠於第5天進行瘢痕切除,以測定肺內病毒載量。B)“主肺炎鏈球菌感染”,每組5隻(見圖),每組2 × 10隻,測定菌血症;C)在“肺炎鏈球菌超感染”,每組10隻小鼠至第10天,第5天每組5隻小鼠獻祭,用於測定肺內病毒載量。在"流感感染"和"肺炎鏈球菌在“超級感染”研究中,小鼠通過鼻內給藥,接受流感病毒株PR8的亞致死劑量(100空斑形成單位或PFU)。1 a和c).在“原發性感染”研究中(圖4)。1 b),進行了一組初步實驗,以確定的數量肺炎鏈球菌殺傷力。65隻(13組,每組5隻)經OM-85或BLANC預處理10 d的小鼠鼻內感染50 μL的白癜風肺炎鏈球菌含有四種不同CFU劑量的細菌溶液樣品:劑量A = 1.4 × 108菌落;劑量B = 7.0 × 107菌落;劑量C = 3.5 × 107菌落;劑量D = 1.75 × 107CFU [20.].相比之下,在“肺炎鏈球菌“超級感染”研究(圖c),肺炎鏈球菌以較低的CFU劑量(1.0 × 105)鼻內注射亞致死劑量(100 PFU)流感病毒株PR8 5天後。每日測量臨床評分(範圍從1到5)、體重和體溫,在流感病毒感染後的第0天至第5天或第10天,以及在流感病毒感染後的第0天至第5天肺炎鏈球菌感染和超級。疾病評分為1的是健康老鼠;疾病評分為2的小鼠表現出不適跡象,包括輕微的脊椎勃起,輕微的步態改變和下床活動增加;疾病評分為3的小鼠表現出強有力的脊柱勃起、腹部收縮、步態改變和不活動的時間;疾病評分為4,前一組小鼠特征增強,但表現出很少的活動,並趨於死亡;一隻死老鼠得了5分。所有實驗均按照《機構指南》和瑞士聯邦和州動物保護法進行。
統計分析
學生的t采用單因素方差分析(無配對,雙尾)或單因素方差分析計算治療組之間的顯著性水平。
結果
OM-85對小鼠流感病毒感染的抑製作用
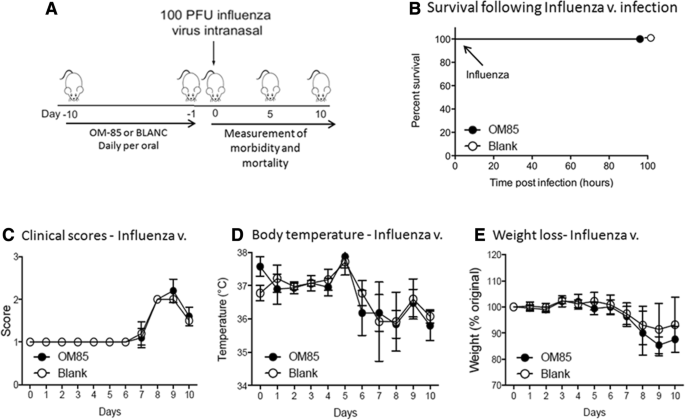
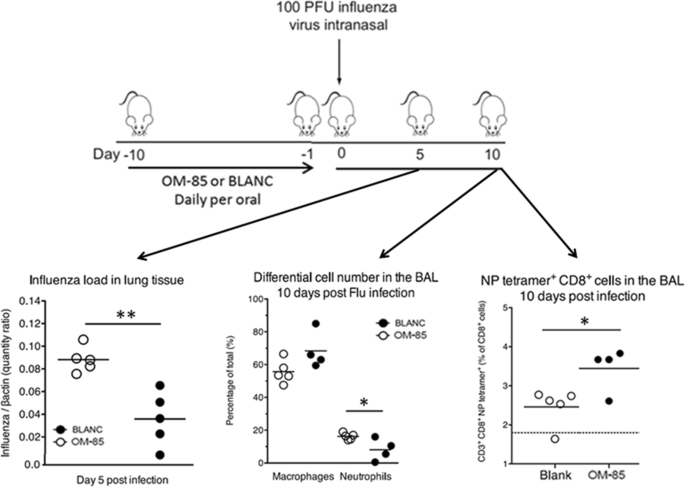
在“病毒感染”實驗中,為了深入了解OM-85是否能增強抗病毒反應,小鼠分別口服OM-85或BLANC 10天。隨後,他們通過鼻內給藥亞致死劑量(100 PFU)的流感病毒株PR8感染(圖。2).獨立於前處理類型(OM-85或BLANC),所有小鼠在第5天都存活(圖。2 b),沒有臨床評分、體重減輕和體溫差異顯示的疾病體征(圖1)。2 c, d而且e).相反,OM-85預處理顯著降低了第5天(感染高峰期)的流感病毒肺水平(p< 0.01),減輕第10天支氣管肺泡灌洗(BAL)中性粒細胞炎症(p< 0.05),這是第5天病毒滴度降低的預期反映(圖5)。3.).有趣的是,OM-85在第10天增加了BAL中np四聚體陽性的流感特異性CD8+ t細胞的比例(p< 0.05),證明免疫係統的適應性臂增強,從而改善了對流感病毒感染的控製(圖。3.).
OM-85對肺炎鏈球菌感染小鼠
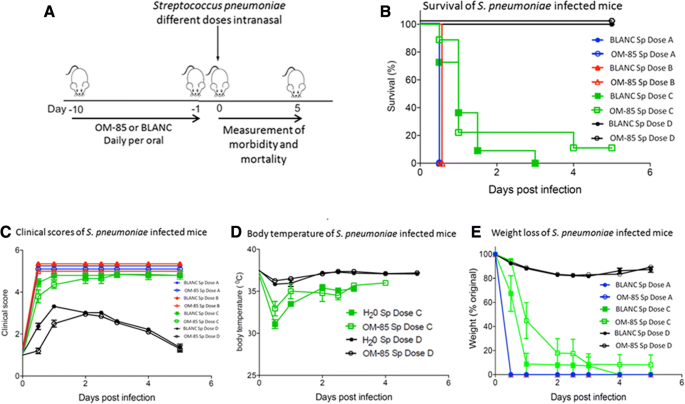
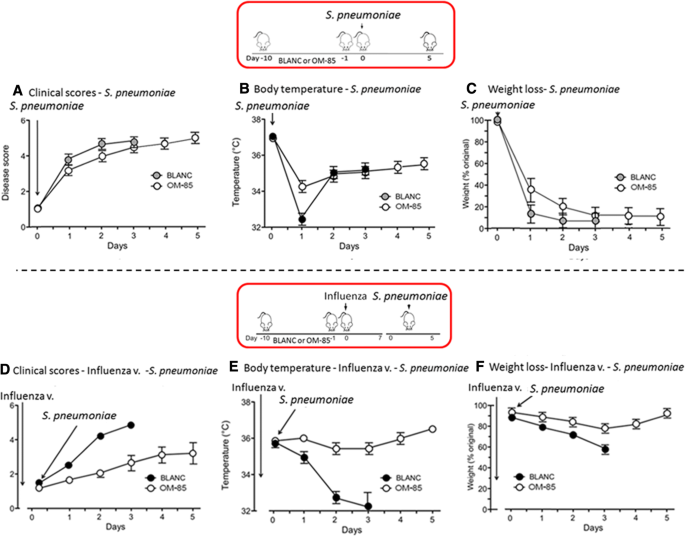
在“原發感染”實驗中,為了深入了解OM-85是否能增強抗菌反應,小鼠分別口服OM-85或BLANC治療10天,隨後用不同劑量的肺炎鏈球菌(無花果。4).獨立於預處理類型(OM-85或BLANC),兩者最高肺炎鏈球菌感染劑量(A和B)是高度致死的,所有小鼠在最初12小時內死亡(圖。4 b).相比之下,C劑量治療的所有小鼠(3 × 107)在使用BLANC治療的第3天死亡,而使用OM-85預處理的小鼠中有20%在第3天存活,10%持續到第5天。相反,當暴露在最低劑量時,所有小鼠都存活到第5天肺炎鏈球菌劑量(D)。盡管不同動物組的小鼠數量較少,且實驗排除了可靠的統計評價,但臨床評分反映了生存數據,表明OM-85對被中間體感染的小鼠具有保護作用肺炎鏈球菌劑量(C)(圖4 c, d而且e).
OM-85在“原發性”與“超級感染”研究中的療效
在這些實驗中,小鼠暴露於亞致死流感感染,然後是次級的,較低的肺炎鏈球菌劑量(1 × 105細菌感染。與之前唯一的“原發感染”研究相比(圖。5而且c),在“超級感染”研究中,om -85治療的小鼠存活率得到了更大程度的提高(圖5)。5 b而且d).第3天,OM-85組成活率為80%,BLAC組為30%;第4天,BLANC組小鼠全部死亡,OM-85組小鼠存活率為70%,第5天仍為50%。當臨床評分時,檢測到相似的結果(圖。6而且d)、體溫(圖。6 b而且e)和體重減輕(圖5。6攝氏度而且f)進行評估。值得注意的是,在暴露後的第1天和第2天,對臨床評分和體溫的積極影響已經被檢測到和明顯肺炎鏈球菌,表明宿主對細菌感染立即產生免疫反應。
討論
OM-85是一種生物來源的口服藥物:其活性原理是一種堿性水溶性萃取物,提取自最初分離自呼吸道感染患者的7屬21種細菌裂解物[21].幾項研究強調了OM-85觸發針對不同病原體的免疫調節和保護性免疫反應的能力,最近,旨在解剖其體外和體內作用模式的連續實驗研究已與科學界分享[16,20.,22,23,24,25,26,27,28,29,30.,31,32,33,34].以細菌和病毒起源的感染為重點,在動物或人類細胞模型上的研究揭示了這類產物能“什麼”和“如何”調節宿主免疫反應的新見解[24,26,33,34].最近的文獻表明,細胞激活發生在腸道相關的淋巴組織中,然後通過淋巴循環遷移到肺相關的淋巴組織[20.,30.,33,35].通過人體取樣原位分析,進一步研究OM-85對病毒感染的保護活性。更準確地說,使用對照和RTI供體疾病樣本,在支氣管鏡檢查後來自肺的人原代支氣管上皮細胞(BECs) [36].在最後的研究中,通過在BECs表麵產生多種抗病毒蛋白來證實其抗病毒機製,其中抗病毒的β-防禦素就是其中的一種。本事後分析的第一個相關發現是,在狹窄的感染劑量窗口內發生了致死性。盡管事實是中級/低肺炎鏈球菌使用BLANC治療的小鼠死亡率較高,且伴隨所有的發病體征。OM-85處理能產生一定的保護作用;然而,這還不足以將易感性降低到致死閾值以下。然而,在最初的研究中,當小鼠首先暴露於亞致死流感感染時[20.], OM-85預處理導致了更相關的預防肺炎鏈球菌感染,如存活率提高和發病率降低所示。在最初的研究中,OM-85在亞致命性流感感染後產生了更相關的保護作用肺炎克雷伯菌超級(20.].這些發現表明對繼發性細菌感染的抵抗力有所提高,這可能隻是部分解釋了低致死率肺炎鏈球菌劑量使用。然而,對OM-85誘導的流感病毒感染的非特異性宿主免疫反應發揮了重要作用[20.].事實上,正如本文前麵所舉的例子,OM-85可以:a)引起樹突狀細胞和b細胞的成熟,同時上調表麵表達MHC II、CD40和CD86 [20.,33b)多克隆激活b細胞,血清中IgG水平有統計學意義的增加,氣道中IgA和IgG水平有增加的趨勢;c)抗i.v.。血清和BAL抗體[20.].病毒感染後對宿主防禦的非特異性刺激的保護作用在觀察中得到了明確的證明,在OM-85治療的小鼠(而不是BLANC治療的小鼠)中,在超感染後24小時肺炎鏈球菌,不再檢出菌血症[20.].考慮到一些重要的發現,原發性病毒感染提高了OM-85對宿主中傳入的細菌感染的有效性,承認這種事後分析的一些局限性是公平的。一個原因是這些數據大多來自動物,由於實驗方法的複雜性和體內條件的不同,使用的小鼠數量有限。另外一個限製也可能源於對流感病毒和的選擇肺炎鏈球菌,通常用於研究小鼠呼吸道合並感染的病原體[37,38],但通常不涉及兒童複發性呼吸道感染。盡管存在這些局限性,但必須強調的是,OM-85的抗菌效果已被證明對其他細菌具有抗菌效果[20.,21].與此同時,OM-85的抗病毒作用最近被證實,其機製證據來自鼻病毒感染的人原代肺細胞[36].我們的事後分析結果支持OM-85 BV在預防兒童和青少年複發性呼吸道感染方麵的臨床療效,通過meta分析和係統綜述顯示[15,16,18,21].從轉譯的角度來看,這些實驗結果支持在兒科常見的呼吸道病毒和細菌超級感染的臨床環境中使用OM-85 BV等免疫調節藥物的概念。雖然病毒(如鼻病毒、腺病毒、副流感病毒和流感病毒)是呼吸道感染的主要原因,但呼吸道病原體(如呼吸道感染)持續的細菌超級感染。肺炎鏈球菌,流感嗜血杆菌化膿性鏈球菌在這一年輕人群中,高達60%的患者被診斷為長期(> ~ 10天)RTI症狀[39].病毒和細菌(通常是流感病毒和細菌)之間的協同作用肺炎鏈球菌)在RTI的發病機製中亦有文獻描述[37,38,39,40].盡管流感可能是致命的,但眾所周知,在細菌過度感染的情況下,死亡率會增加[40].因此,所描述的臨床前觀察結果解釋了OM-85 BV在預防兒童和青少年呼吸道感染、減輕症狀嚴重程度和持續時間以及減少缺課天數方麵的臨床療效,正如係統綜述和meta分析所顯示的那樣[15,16,18,21].減少與較高發病率、抗生素處方、轉介專家就診和住院有關的細菌並發症,也有助於控製衛生保健費用[41].
參考文獻
社區獲得性下呼吸道感染:病因學和治療。胸部。2001;120:2021-34。
Heikkinen T, Järvinen A.普通感冒。《柳葉刀》雜誌。2003;361:51-9。
布雷利JC,希爾PD,楊PR,查佩爾KJ。兒童早期呼吸道的病毒性細菌合並感染。微生物學通報,2015;362(10):fnv062。https://doi.org/10.1093/femsle/fnv062.
Ghoneim HE, Thomas PG, McCullers JA。肺泡大泡衰竭一個流感感染期間的Ges促進了細菌的重複感染。J Immunol。2013;191:1250-9。
Avadhanula V, Rodriguez CA, DeVincenzo JP, Webby RJ, Ulett GC,等。呼吸道病毒以一種依賴於病毒種類和細胞類型的方式增強細菌病原體對呼吸道上皮的粘附。J微生物學報。2006;80:1629-36。
先天性免疫變阻器對肺部炎症性疾病和繼發性細菌性肺炎的影響。生物化學學報2009;37:811-3。
久樹H,石田N,深澤C,星野T,相澤J,石川N,等。兒科住院患者呼吸道合胞病毒合並感染支氣管肺感染的發生率。《感染化學雜誌》2011;17:87-90。
McCullers JA, McAuley JL, Browall S, Iverson AR, Boyd KL, Henriques Normark B.流感增強了雪貂對肺炎鏈球菌自然獲得和疾病的易感性。中華傳染病雜誌2010;202:1287-95。
新生兒的先天免疫:基本機製和臨床相關性。免疫免疫學雜誌2007;7:379-90。
Klaenhammer TR, Kleerebezem M, Kopp MV, Rescigno M.益生菌和益生元對免疫係統的影響。免疫免疫學雜誌2012;12:728-34。
農場生活對兒童哮喘和過敏的影響。免疫免疫學雜誌2010;10:861-8。
Pfefferle PI, Prescott SL, Kopp M.微生物對耐藥性的影響和益生元/益生菌和細菌裂解物幹預的機會。過敏臨床免疫雜誌2013;131:1453-63。
Stein MM, Hrusch CL, Gozdz J, Igartua C, Pivniouk V, Murray SE,等。阿米什和赫特人農場兒童的先天免疫和哮喘風險。中華醫學雜誌2016;375:411-21。
Del-Rio-Navarro BE, Espinosa-Rosales FJ, Flenady V, Sienra-Monge JJL。預防兒童呼吸道感染的免疫刺激劑。基於證據的兒童健康,2012;7:629-717。
Kearney SC, Dziekiewicz M, Feleszko W.細菌裂解物在呼吸道感染和哮喘中的免疫調節和免疫刺激反應。Ann Allergy Asthma Immunol 2015; 114:364-9。
Schaad烏蘭巴托。OM-85 BV,一種用於兒童反複呼吸道感染的免疫刺激劑:一項係統綜述。世界兒科雜誌2010;6:5-12。
Razi CH, Harmanci K, Abaci A, Özdemir O, hazllah S, Renda R, Keskin F.免疫刺激劑OM-85 BV可預防學齡前兒童喘息發作。過敏臨床免疫雜誌2010;126:763-9。
尹靜,徐波,曾曉,沈坤。支氣管-瓦克鬆治療小兒反複呼吸道感染:一項係統綜述和薈萃分析。Int Immunopharmacol。2018;54:198 - 209。
唐紅,方錚,Saborío GP,秀瓊。OM-85在慢性支氣管炎和/或慢性阻塞性肺疾病患者中的療效和安全性。肺。2015;193:513-9。
Pasquali C,薩拉米O, Taneja M, Gollwitzer ES, Trompette A, Pattaroni C等。增強粘膜抗體的產生和保護呼吸道感染後,口服細菌提取物。醫學。2014;一41。
Esposito S, Soto-Martinez ME, Feleszko W, Jones MH, Shen KL, Schaad UB。兒童反複呼吸道感染、喘息和哮喘的非特異性免疫調節劑:一項機製和臨床證據的係統綜述。《過敏臨床免疫雜誌》2018;18:19 19 - 209。
張強,王磊,王超,徐旭,等。OM85-BV通過TLR4和tlr2介導的ERK1/2/NF-κ b通路誘導RAW264.7細胞產生IL-1β、IL-6和TNF-α。中華細胞因子雜誌2014;34:526-36。
細菌提取物(OM-85 BV)激活人體內自然殺傷細胞和細胞因子的產生。肺。1990;168:720-5。
M街,LH座。支氣管- vaxom (OM-85 BV)對gp130結合細胞因子的顯著影響。胸腔。2000;55:678 - 84。
Keul R, Roth M, Papakonstantinou E, Nauck M, Perruchoud AP, LH座。支氣管- vaxom (OM-85 BV)通過C-Fos/血清反應元件誘導白細胞介素6和白細胞介素8的表達。胸腔。1996;1:150-4。
Dang AT, Pasquali C, Ludigs K, Guarda G. OM-85是一種幹擾素-β產生和炎症小體活性的免疫調節劑。Sci眾議員2017;7:43844。
Bessler WG, Kleine B, Martinez Alonso C, Biesert L, Strecker M, Wiesmüller KH,等。細菌表麵成分的生物活性:作為免疫調節劑的細菌提取物和細菌細胞壁成分。肺。1990;168:707-15。
Bessler WG, Huber M, Baier W.作為免疫調節劑的細菌細胞壁成分。2細菌細胞壁提取om - 85bv作為小鼠非特異性激活劑、免疫原和佐劑。國際免疫藥物雜誌,1997;19:551-8。
胡貝爾M,莫斯曼H,貝斯勒WG。細菌提取物OM-85-BV的th1定向免疫特性。歐洲醫學雜誌2005;10:209-17。
細菌提取物OM-85 BV能保護小鼠免受流感和沙門氏菌感染。Int Immunopharmacol。2010;10:1086 - 90。
口服細菌提取物對免疫未成熟大鼠係統性Th1免疫的選擇性增強。感染Immun。2001;69:3719-27。
Navarro S, Cossalter G, Chiavaroli C, Kanda A, Fleury S, Lazzari A,等。口服細菌提取物通過將調節性T細胞招募到氣道來預防哮喘。粘膜Immunol。2011;4 - 65。
Parola C, Salogni L, Vaira X, Scutera S, Somma P, Salvi V,等。OM-85通過NF-kB和MAPK依賴通路選擇性激活人樹突狀細胞《公共科學圖書館•綜合》。2013;8:e82867。
Evans SE, Scott BL, Clement CG, Larson DT, Kontoyiannis D, Lewis RE,等。受刺激的肺上皮細胞的先天抵抗力可廣泛保護小鼠免受細菌和真菌的侵害。中華呼吸細胞生物學雜誌2010;42:40-50。
Manalova V, Face A, Jeandet P, Bessler WC, Pasquali C.免疫調節劑細菌提取物OM-85誘導的生物標誌物:對Peyer 's patches和腸上皮細胞的獨特作用中華臨床細胞免疫雜誌2017;8:494。
Roth M, Pasquali C, Stolz D, Tamm M. Broncho Vaxom (OM-85)通過Erk1/2有絲分裂原激活蛋白激酶和cAMP調節鼻病毒在人氣道上皮細胞上的對接蛋白。《公共科學圖書館•綜合》。2017;12:e0188010。
Moore DP, Dagan R, Madhi SA。呼吸道病毒和肺炎球菌合並感染:肺炎球菌疫苗接種的意義。專家Rev呼吸醫學2012;6:451-65。
李輝,陳旭,周世傑。達烏利辛聯合克林黴素可抑製H5N1型流感病毒和克林黴素合並感染的重症肺炎Strepotococcus肺炎在體外和體內通過NF-kB信號通路。中國藥學雜誌2018;137:12-9。
Salami A, Dellepiane M, Crippa B, Mora F, Guastini L, Jankowska B,等。吸入含硫水在預防反複上呼吸道感染中的作用。中華兒科耳鼻喉雜誌2008;72:1717-22。
她從來農協。洞察流感病毒和肺炎球菌之間的相互作用。臨床微生物學修訂版2006;19:571-82。
免疫刺激劑OM-85預防小兒反複上呼吸道感染的經濟分析。Glob Reg健康技術評估。2015;DOI:https://doi.org/10.5301/GRHTA.5000200.
Wark PAB, Ramsahai JM, Pathinayake P, Malik B, Bartlett NW。呼吸道病毒和哮喘。Semin呼吸危重護理醫學2018;39:45-55。
羅西GA,科林AA。嬰兒呼吸道合胞病毒和人鼻病毒感染:各自在喘息的開始和持續中的作用。歐洲呼吸科學雜誌。2015;45:774-89。
Wedzicha農協。慢性阻塞性肺疾病加重機製。2015;12: S157-9。
馬丁內斯FD,維切利d。哮喘。《柳葉刀》雜誌。2013;382:1360 - 72。
Lehtinen P, Jartti T, Virkki R, Vuorinen T, Leinonen M, Peltola V,等。病毒性喘息患兒的細菌性合並感染。中華臨床微生物感染雜誌2006;25:463-9。
學齡前複發性喘息和哮喘的管理:基於表型的方法。《過敏臨床免疫學》2017;17:131-8。
資金
最初的研究由瑞士日內瓦Vifor製藥集團的OM Pharma SA公司資助,由瑞士洛桑epallings合同研究組織precin Biosystems執行。隻有首席科學官和本報告的最後一位作者參與了研究的設計、數據收集和分析。
數據和材料的可用性
目前研究期間分析的數據集可在:a) Broncho Vaxom™(OM85): 135.414 -中試研究- bv2012 /6,“流感後的細菌超級感染”;b) Broncho Vaxom™(OM85): 135.414裏程碑1和2 BV2012/7,“流感後亞致死細菌超級感染”;c)最終科學報告Broncho-Vaxom™(OM85): 135.442, BV2012/11,“流感後細菌超級感染的重複”。
作者信息
作者和聯係
貢獻
所有的作者都參與了數據的分析和解釋,並為撰寫稿件做出了貢獻。所有作者閱讀並認可最終稿件。
相應的作者
道德聲明
倫理批準
動物實驗是根據《機構準則》和瑞士聯邦和州動物保護法進行的。
同意出版
不適用
相互競爭的利益
G.A. Rossi是瑞士日內瓦Vifor製藥集團的OM Pharma SA公司的活躍顧問;W. Bessler是德國弗賴堡的名譽教授和特邀嘉賓;S. Ballarini是瑞士日內瓦Vifor Pharma Group旗下公司OM Pharma SA的員工;C. Pasquali是瑞士日內瓦Vifor Pharma Group旗下公司OM Pharma SA的員工。
出版商的注意
beplay外围下载施普林格自然對出版的地圖和機構附屬的管轄權要求保持中立。
權利和權限
開放獲取本文根據創作共用署名4.0國際許可協議發布(http://creativecommons.org/licenses/by/4.0/),該協議允許在任何媒體上不受限製地使用、分發和複製,前提是您適當地注明原作者和來源,提供創作共用許可的鏈接,並說明是否有更改。創作共用公共領域奉獻放棄書(http://creativecommons.org/publicdomain/zero/1.0/)除另有說明外,適用於本條提供的資料。
關於這篇文章
引用這篇文章
羅西,G.A,貝斯勒,W,巴拉裏尼,S。et al。有證據表明,OM-85對免疫反應的初級抗病毒刺激降低了小鼠對繼發性呼吸道細菌感染的易感性。斜體字J Pediatr44112(2018)。https://doi.org/10.1186/s13052-018-0569-7
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-018-0569-7
關鍵字
- 呼吸道感染
- 細菌中提取
- 鏈球菌引起的肺炎
- 流感病毒
- 適應性免疫