摘要
背景
胎兒在子宮內的規劃決定了導致成年的生理和代謝反應的設定值;在"頭1 000天"(從懷孕到2歲)發生的事件在非傳染性疾病的發展中發揮作用。嬰兒腸道微生物群是一個高度動態的器官,對母體和環境因素敏感,是推動非傳染性疾病代際傳播的因素之一。
A.MA.MI (Alimentazione MAmma e bambino nei primi MIlle giorni)項目旨在調查從受孕到出生第一年的幾個因素與嬰兒腸道微生物組組成之間的相關性。我們描述了A.MA.MI研究的研究設計,並提出了一些初步結果。
方法
A.MA.MI是一項縱向、前瞻性、觀察性研究,針對一組母嬰(n= 60)參加帕維亞(意大利)聖馬特奧紅十字會基金會新生兒病房。本研究計劃分別提供出院前T0、T1、T2、T3、出生後1、6、12個月的數據。
每次評估產婦和嬰兒的人體測量值。評估的其他變量包括:孕前/妊娠體重狀況(T0)、母親飲食習慣/體力活動(T1-T3);嬰兒病史、喂養類型、抗生素/益生菌/補充劑使用、環境暴露(如吸煙、寵物、環境溫度)(T1-T3)。計劃每次收集嬰兒糞便樣本,采用宏基因組學16S核糖體RNA基因測序方法進行分析。
結果
分娩方式(剖宮產vs.陰道分娩)和孕婦孕前BMI (BMI < 25 Kg/m2vs. BMI≥25 Kg/m2),屬和種水平差異顯著(T0)。在喂養類型(母乳喂養與配方奶喂養)上,腸道菌群組成在屬和種水平上存在顯著差異(T1)。
結論
這些初步和探索性的結果證實,孕前、分娩方式和嬰兒因素可能在不同程度上影響嬰兒微生物群組成。
試驗注冊
ClinicalTrials.gov標識符:NCT04122612.
背景
從巴克假說開始,認識到編程現象不僅與胎兒生命有關,而且與發育有關,可以追溯到胚胎早期,並向前延伸到嬰兒期和幼兒期,從而產生了健康與疾病的發育起源(DOHaD) [1].
DOHaD理論的證據指出了支持肥胖、2型糖尿病、癌症、呼吸係統疾病等非傳染性疾病代際性的生物機製,這些疾病在大多數國家都是一個日益嚴重的公共衛生問題[2,3.].此外,科學證據證實,在生命早期階段發生的事件在促進整個生命過程中慢性疾病的發展方麵起著關鍵作用,這表明"母體環境"對未來兒童生活的影響具有高度相關性[4,5].這段影響後代未來健康的關鍵時期被稱為“前1000天”,從受孕開始,一直持續到兩歲。
推動非傳染性疾病代際性並在“最初1000天”中發揮關鍵作用的關鍵因素之一是腸道微生物組,這是一種高度動態的器官,對環境因素敏感,並在宿主的一生中改變其組成[6].
細菌建立過程是一個複雜的現象,始於子宮內:在過去,宮內環境被認為是無菌的,但最近的證據支持宮內母體到胎兒的微生物交換,挑戰了一個多世紀以來在世界範圍內公認的傳統“無菌子宮”[7,8,9].大多數腸道微生物要麼是無害的,要麼對宿主有益,可以抵禦入侵的病原體;腸道微生物組內正常平衡的破壞(也稱為生態失調)與非傳染性疾病的發展有關[10].
因此,了解調節維持平衡微生物組的潛在機製可能因此具有治療意義或導致降低非傳染性疾病發展風險的策略[10].
已知有許多因素會影響嬰兒出生第一年腸道微生物群的多樣性和結構,例如懷孕前的母體因素(例如體重指數和體重波動)[11],妊娠暴露[12,13,14,15](例如產婦生活方式、體重增加、病理生理狀況、補充劑使用、抗生素接觸、汙染物接觸)、分娩方式[16,17]及喂食方式[18],從而引發腸道微生物群失調[19].
眾所周知,懷孕期間體重過度增加是影響新生兒到成年期腸道微生物組成的產婦因素之一[11]和之前的人類研究表明,與體重正常的母親所生的孩子相比,懷孕期間肥胖或超重的母親所生的孩子在生命的不同階段腸道微生物組成存在顯著差異[20.,21].
影響新生兒腸道微生物組成的另一個公認的重要因素是孕婦在懷孕期間的飲食習慣[22,23];先前在體內模型中有報道,在不同的動物模型中,懷孕和哺乳期的西方飲食會影響後代腸道微生物群失調[24,25].
幾項研究已經確定了陰道分娩和剖宮產分娩的嬰兒存在不同的腸道微生物譜[26],與順產出生的嬰兒相比,選擇性剖宮產出生的嬰兒中微生物群落的豐富度和多樣性較低[26].
孕產婦微生物組組成的變化也可以垂直轉移給新生兒,不僅在出生時,而且在哺乳期間,促進改變微生物群落的接種,這可能會產生短期和長期的健康後果[27].此外,喂養方式(配方奶或母乳喂養)似乎對腸道微生物組成有很大的影響,除了圍產期等因素,包括分娩方式、胎齡和母親體重狀況以及生活方式,都會影響母乳中的微生物和非微生物成分,影響嬰兒腸道和健康[28].此外,有證據表明,母乳喂養能夠預防生態失調和其他疾病(即自身免疫和過敏性疾病)的發生,世界衛生組織(世衛組織)確實建議嬰兒在出生後的前6個月應純母乳喂養[29].此外,不同個體之間腸道微生物組的差異有兩個主要組成部分需要考慮:年齡引起的變化和飲食變化直接引起的影響[30.].
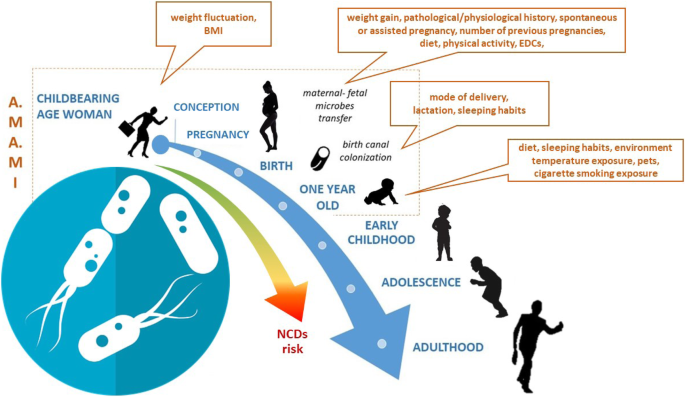
基於上述所有考慮因素,ama . mi (Alimentazione MAmma e bambino nei primi MIlle giorni)項目的目的是在不同的隨訪中,調查出生一年內母親產前和妊娠暴露因素、分娩方式、哺乳、家庭環境、嬰兒飲食、睡眠習慣和嬰兒腸道微生物組組成之間的可能相關性(圖。1).
A.MA.MI研究的概念框架,改編自Stiemsma等人[8]
在本研究文章中,描述了A.MA.MI的研究設計和整個方案。此外,我們提出了一些初步和探索性的結果,關於調查出生嬰兒的腸道微生物組組成在生命的第一個月。
方法
研究設計和目的
A.MA.MI是一項縱向前瞻性觀察性研究,包括從出生到1歲的母嬰對(成對),旨在:
- 1)
主要結果:通過以下方法調查嬰兒(0-11.99個月)腸道微生物組的發育:i)確定優勢微生物的相對豐度,ii)評估微生物多樣性,iii)評估個體間變異。
- 2)
次要結果:在不同的隨訪中,探索懷孕前母親因素(體重狀況)、妊娠暴露(母親飲食、身體活動、體重狀況)、分娩方式、喂養方式(配方奶或母乳喂養)、家庭環境暴露、嬰兒飲食、睡眠習慣和嬰兒腸道微生物組組成之間的可能相關性:
交貨後立即(交貨後不超過2天,T0);
出生後1個月(T1);
出生後6個月(T2);
出生後12個月(T3)。
該研究得到了帕維亞基金會(Fondazione IRCCS Policlinico S. Matteo)人類倫理委員會的批準(協議號:20180022618;2018年6月12日),並根據良好臨床實踐指南進行。提供父母/法定監護人的書麵知情同意。帕維亞的IRCCS Policlinico S. Matteo基金會的人類倫理委員會批準了這一程序。
參與者
在本研究中,開始招募63對雙胞胎,目的是完成至少50對母嬰(母親/新生兒)的研究,參加帕維亞(意大利)聖馬特奧基金會IRCCS Policlinico新生兒部門,並根據以下入選標準:
由自然分娩或剖腹產而生的男女嬰兒;
胎齡在37 - 42周之間;
意大利語流行的父母;
父母/監護人給予知情同意的能力;
母親對結構化訪談/問卷的回答能力;
排除標準:
患有遺傳/先天性疾病的嬰兒或母親;
嬰兒出生後立即住進新生兒重症監護室;
入選其他臨床研究的嬰兒;
存在妊娠期糖尿病;
懷孕期間有甲亢;
分娩前,在母親的例行探視中,告知父母/法定監護人研究的性質和他們積極參與的可能性,然後,他們被邀請簽署知情同意書。
根據美國婦產科醫師學會(ACOG) 2019年指南進行分娩期間抗生素預防[31].
問卷調查和訪談
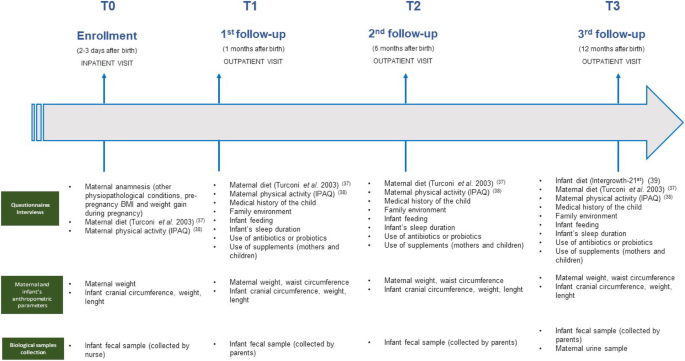
所有數據收集的時間軸如圖所示。2.
在T0階段,研究小組訓練有素的人員對母親進行了訪談,內容包括:
她們的病理/生理史、懷孕信息(當前懷孕類型、自發或輔助懷孕、以前懷孕次數)和人體測量參數(身高、懷孕前後體重、懷孕前後體重指數(BMI));
他們的飲食習慣通過事先驗證過的問卷調查[32];
他們的體育活動習慣,通過事先驗證的問卷調查[33].
在T1、T2、T3對母親進行訪談,內容為:
兒童病史、家庭環境(家中有多少人、是否養寵物、體溫、家庭社會經濟水平、嬰兒是否被動吸煙)、喂養方式(配方奶或母乳喂養)、斷奶時間和特點、嬰兒睡眠時間、母親和兒童是否使用抗生素或益生菌以及是否使用補充劑;
他們的飲食習慣通過事先驗證過的問卷調查[32].
他們的體育活動習慣,通過事先驗證的問卷調查[33].
為了調查嬰兒在1歲時的飲食習慣,在T3也會對母親進行訪談,方法是使用先前驗證過的問卷[34],采用前後平移法(https://www.who.int/substance_abuse/research_tools/translation/en/).
特別是,為了調查母親的飲食(T0-T3),以前驗證過的問卷的改編版本[32]已被確認並分發給這些母親。
食物頻率部分(FF)評估典型食品和飲料的日常消費量,如意大利麵、穀物產品、麵包、蔬菜和水果、牛奶和酸奶,以及肉類和肉類衍生物、豆類、魚類、雞蛋和奶酪的每周消費量;酒精飲料、糖果及甜點的消耗量亦被調查[32].飲食習慣組調查與進食頻率、份量、用水量、軟飲及含酒精飲料有關的飲食習慣[32].每個部分由以下回答類別的問題組成:總是,經常,有時,從不。根據國家膳食指南[35].
為調查體育活動,經驗證的體育活動和久坐行為評估問卷的簡短版本(國際體育活動問卷,IPAQ) [33]被收養。IPAQ是為成年人(年齡範圍為15-69歲)的身體活動監測而開發和測試的工具。IPAQ簡短版(7項)的結構是提供有關在劇烈、中等強度活動、步行和久坐活動中所花費時間的信息和單獨分數。簡短形式的總分估計需要這些活動的頻率(天)和持續時間(分鍾)的總和;每項活動都用METs定義的能量需求來表示,並以met分鍾為單位進行評分。
所選MET值由Ainsworth等人獲得。綱要(36]並且每一項活動都達到MET平均分。例如,包括所有類型的步行,並為步行創建一個中等MET值。同樣的方法用於中等強度和高強度的活動。請注意,關於休息時間的問題是作為單獨的指標製定的,而不是作為體育活動總分的一部分。
最後,為了調查嬰兒在1歲(T3)時的飲食習慣,使用了以前驗證過的問卷的改編版的兩個部分[34].第1部分調查嬰兒在出生後一年內的喂養情況,而第2部分由食物頻率問卷組成,用於評估過去28天內的食物消耗[34].
母嬰的人體測量參數
計劃在T0-T3測量孕婦身高(cm)、體重(kg)、BMI (kg /m)等人體測量參數2)然後計算;計劃在T1-T3測量腰圍(WC) (cm)(圖。1).
體重和身高都是按照標準程序測量的。在母親隻穿內衣不穿鞋的情況下,用杆秤測量體重(精度±100 g);用身高儀測量不穿鞋母親的身高(精度±1 mm)。參與者站立,雙臂交叉,雙手放在相對的肩膀上,用柔性鋼卷尺測量腰圍,精確到厘米。輕輕呼氣後,在胸腔最低部與右髂骨最外側邊界之間的水平麵上測量腹部WC [37].
BMI也被計算為體重和身高的平方與體重(公斤)和身高(米)之比[37].
每個患兒計劃在出院前(T0)、1個月(T1)、6個月(T2)和1歲(T3)時進行隨訪(圖3)。1).嬰兒體重(kg)、體長(cm)及頭圍(cm)均采用標準化程序測量(T0-T3) [37].
用杆秤測量嬰兒體重(精度±100 g)。將嬰兒放在嬰兒計上,雙腳朝向活動腳件,頭部靠在固定頭件上,由檢驗員測量長度,檢驗員將腳放好並確保頭部位於法蘭克福水平麵上。如果不可能在正確的位置上伸展雙腿,考官確保至少一條腿是伸直的,腳彎曲靠在腳片上。
使用無拉伸量尺測量嬰兒頭圍至最接近1mm,將卷尺放置在嬰兒頭部周圍,膠帶貼在顱骨額骨上;略高於眉毛;垂直於臉的長軸的;耳朵以上;並在後腦枕凸上方,根據標準評估方法,在後腦上方上下移動膠帶,以確定最大圍度,並收緊插入膠帶,使其完全貼合頭部,並壓迫頭發和下麵的軟組織[37].
樣品收集
將每個嬰兒的糞便樣本(T0 - T3)收集到2個不同的螺旋頂容器中,並標記上新生兒唯一的研究ID號。一份樣本保存在−80°C的新生兒重症監護室,IRCCS Policlinico San Matteo基金會(意大利帕維亞);另一份保存在帕維亞大學(意大利帕維亞)醫學院公共衛生實驗和法醫學係人體解剖研究所,溫度為- 80°C,直到進行分析。
特別是在T0時,一位訓練有素的護士收集了新生兒的糞便樣本。在訪問結束時,研究小組的一名成員安排了第二次well-child-visit(出生後1個月,T1),並向父母/法定監護人提供了用於收集新生兒第二次糞便樣本的工具包。父母/法定監護人也被指導如何在家中獨立收集糞便樣本。
在T1預定訪視前1-2天由研究小組成員聯係新生兒父母,檢查新生兒健康狀況;此外,他們還被要求在其他時間提交糞便樣本,如果:
兒童目前有發燒、呼吸道疾病或腸胃疾病;
兒童在過去7天內有持續超過24小時的腹瀉症狀;
兒童在過去7天內曾接受抗生素治療。
另外2次隨訪(T2、T3)大便標本采集均按相同流程進行。
樣品分析
糞便樣本用幹冰運送到Genomix 4 Life Srl (C/O分子和基因組醫學實驗室-意大利薩萊諾的Baronissi醫學和外科校園,意大利費西亞諾薩萊諾大學的分支),在那裏進行16S宏遺傳分析。樣本隻有研究ID號;這些樣本沒有附帶臨床或個人信息。
糞便DNA提取
根據製造商的說明,使用QIAamp®快速DNA糞便迷你試劑盒(QIAGEN, Hilden, Germany)從冷凍糞便樣本中分離出總基因組細菌DNA。
16S rrna宏遺傳分析估計腸道菌群
利用Illumina MiSeq平台進行16S宏遺傳分析。擴增16S rRNA基因V3-V4區,分析細菌結構域內的多樣性[38].按照genome ix4life的方案進行PCR和測序分析。質量控製(QC)和分類學分配是根據QIIME和核糖體數據庫項目貝葉斯分類器,結合一組由Genomix4life實現的用於微生物群落分析的定製設計的信息學管道完成的。
在NCBI 16S核糖體RNA序列數據庫中使用BLAST搜索進行分類歸屬[39].對每個樣品分別調查每種細菌操作分類單位(OTUs)的百分比,根據每個樣品內的相對reads數提供樣品之間的相對豐度數據[39].Alpha多樣性(觀測物種、Chao1豐富度和Shannon多樣性指數)采用Qiime變異[40,41]在群體之間的微生物群落中;群落研究采用基於係統發育的非加權Unifrac距離度量[41].
統計分析
動力分析
A.MA.MI研究最初的設想規模相對較小(至少60對),以完成至少50對母嬰的研究,並提供A.MA.MI研究方案的初步可行性(它可能被認為是試點研究)。目的是探索嬰兒微生物組的可變性,並驗證幾種可能與微生物組發育相關的母親和嬰兒因素的影響程度。獲得的信息還將用於更好地確定更大研究的樣本量,以驗證前一項研究的結果。因此,我們將計算和提及因果在初步研究結束時討論具體結果時,要考慮權力。
為了最大限度地減少隨訪過程中的損失,研究人員計劃通過電話提醒參與者所有的隨訪活動。
主要和次要目標分析計劃
數據通過描述性統計的方法進行總結,如適當的定量變量的均值和標準差或中位數和四分位範圍(IQR),定性變量的相對頻率。
為了研究嬰兒腸道微生物的發育情況,采用主成分分析(PCA)和Spearman相關法評估不同隨訪時間內微生物組成的變化。
為了評估腸道微生物組組成與前文所述的母嬰因素之間的關係,已酌情選擇t檢驗/方差分析或Mann-Whitney/Kruskal-Wallis。比較不同門屬的相對豐度和多樣性指數在產前或產後特定因子存在/不存在或不同類別所定義的組間的差異。
為了捕捉較低分類水平的多餘零的特征並對細菌數據的螺旋豐度進行建模,還實現了零膨脹模型並對結果進行了比較。
為了評估腸道微生物組發育與不良生長參數狀況的關係,使用了重複測量方差分析或Friedman檢驗,並對多重比較進行了調整。在群體時間相互作用的情況下,進行了事後多水平混合效應線性回歸檢驗。
最終,為了明確腸道微生物組組成和發育與產前或新生兒因素之間的關係,我們使用了廣義線性模型(GLM),使用適當的鏈接函數將模型與不同的因變量聯係起來。所有回歸模型都可以根據可能的混雜因素進行調整,例如社會人口信息。所有檢驗均為雙尾檢驗,統計學顯著性水平設置為0.05。
所有分析均使用STATA 15進行。
結果
2018年10月開始入組,收集T0、T1和T2的數據和樣本。所有關於T2和T3入學的分析都在進行中。
以下是關於T0和T1嬰兒腸道微生物組組成與母親體重狀況、分娩類型和哺乳的一些初步和探索性結果。
一般特征
在帕維亞(意大利)聖馬特奧市IRCCS Policlinico聖馬特奧新生兒病房共招募了63對雙胞胎,根據一對雙胞胎在入學後退出,四對雙胞胎在T1退出。
表中描述了這對組合的一般特性1.
36名女性(48.1%)是第一次懷孕。大多數女性(96.8%)的受孕類型是自發的,(n= 60),隻有3.2% (n= 2)接受了輔助生殖技術(ART)。85.5%的產婦分娩方式為自然陰道分娩(n= 53)。
58.6%的嬰兒(n= 34),而41.1% (n都是用配方奶喂養的。
嬰兒微生物組分析
初步結果報告描述了新生兒在T0(胎糞)和T1的腸道微生物組組成。
118份新生兒糞便樣本中,通過過濾質量的reads平均為106,298.81±69,276.42個序列。考慮alpha多樣性(已識別物種OTUs的數量)和Shannon多樣性指數(附加文件)分析細菌群落1:表S1)。
新生兒與1個月大嬰兒的比較
T0時OTUs的平均數量大於T1時(p= 0.001),而物種多樣性(Shannon指數)具有可比性(p> 0.05)考慮T0 vs T1。
厚壁菌門、擬杆菌門、變形菌門、放線菌門、梭杆菌門、藍藻門和疣菌門的16S rRNA基因序列占所有樣本的98%以上。相對豐度< 0.1%的序列門被歸為一類,稱為其他人.
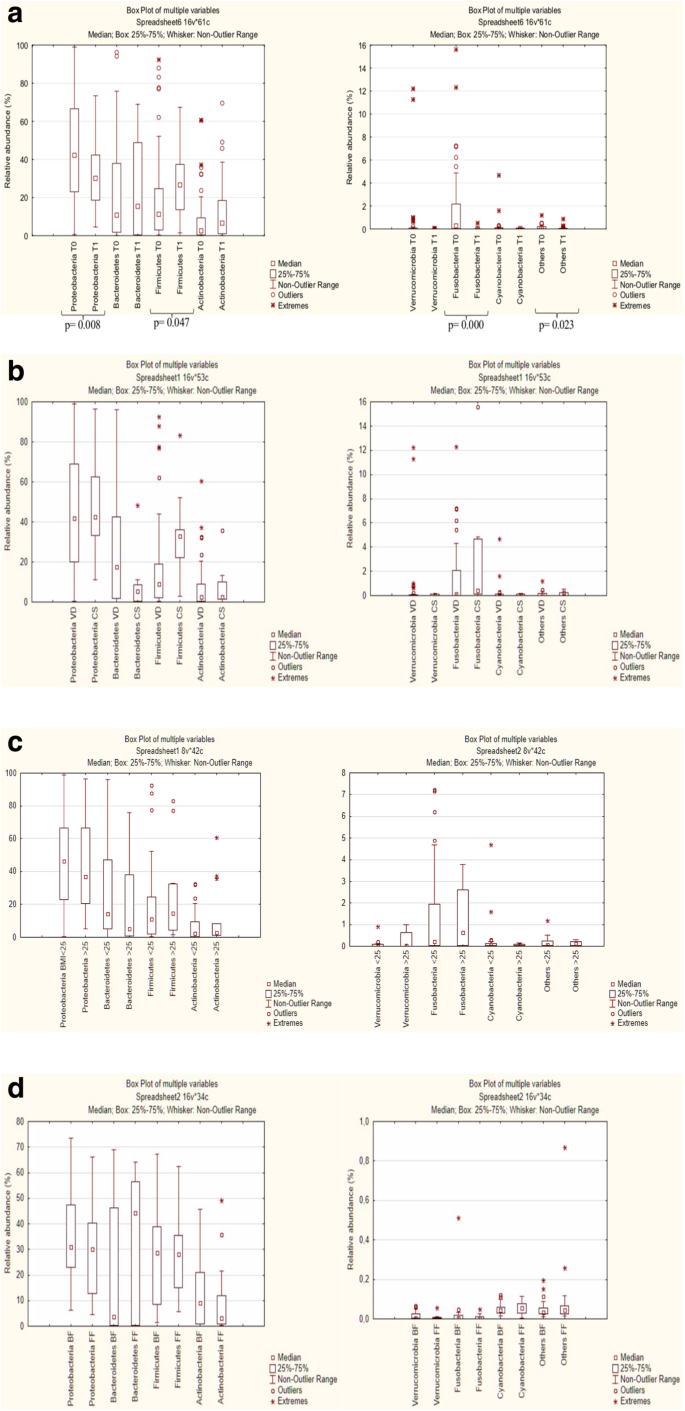
T1時厚壁菌門相對豐度高於胎糞(T0: 19.71%, T1: 27.52%;p= 0.047),與Proteobacteria的減少有關(T0: 46.23% vs. T1: 33.56%;p= 0.008)和梭杆菌(T0: 1.65% vs. T1: 0.02;p= 0.000)3.一個)。
T1時,在屬和種水平上,Fusobacteria屬和種均明顯減少。形核梭杆菌,纖毛菌屬shahii,l . wadei而且Sebaldella;p< 0.001)。這樣,在對所有糞便樣本進行排列分析的聚類1中(圖S1A)以上述屬的數量為正分數為特征。
厚壁菌門、Blautia,乳酸菌物種(l . gasseri而且l . taiwanensis),瘤胃球菌屬(r . gnavus),韋永氏球菌屬(即。V. atypica, V. criceti,而且訴dispar)在T1 (p< 0.035)。
否則,鏈球菌sp在種間表現出不同的趨勢;事實上,一些物種減少了(例如。美國的對象,美國的中間部,美國雜誌而且美國tigurinus) (p< 0.009),而其他物種在出生後30天(T1)增加,包括美國fryi而且美國前庭神經(p< 0.046)。
同樣,放線菌屬的一些屬,即。放線菌,棒狀杆菌屬,分枝杆菌,Parascardovia,丙酸菌屬,羅思氏菌屬與胎糞相比T1下降(p< 0.041)。另一方麵,Collinsella(t0: 0.05%, t1: 0.56%;p= 0.047),特別是雙歧杆菌屬放線菌屬(T0: 1.93%, T1: 12.39%;p= 0.000),如對所有糞便樣本進行排列分析的聚類2所示(圖S1a).同時,比較集群1(圖S1a),主要包括t0樣本,到聚類2,包括98.25%的t1樣本(56/57),觀察到幾個變形菌門物種在出生後明顯減少,包括Burkholderiaceae (Lautropia spp。而且Ralstonia spp。)及水仙科(Kingella spp。而且奈瑟氏菌屬。),以及Bradyrhizobiumspp。彎曲杆菌spp。Methylobacteriumspp。Oxalobacter(特別是o . vibrioformis),假單胞菌spp。(特別是p . brenneri) (p< 0.037)。相反,隻是Trabulsiella(腸杆菌科),Sutterella變形菌門(Sutterellaceae)均高於胎糞(p< 0.048)。擬杆菌門屬間無明顯增加,而擬杆菌門屬間無明顯增加Capnocytophaga,Chryseobacterium,Porphyromonas,普氏菌,TannerellaT1低於T0 (p< 0.011)。
T0時分娩方式的比較:陰道分娩與剖宮產
在門水平上,剖宮產(CS)和陰道分娩(VD)的新生兒胎糞沒有統計學差異(圖2)。3.b).兩個樣本類群之間的主要差異在屬和種水平上。
經CS出生的新生兒胎糞中厚壁菌門(Firmicutes)屬和種均高於VD,其中以乳酸菌科(lactobacillus aceae)最為明顯乳酸菌而且片球菌屬,芽孢杆菌(特別是b . butanolivorans),月形單胞菌屬(artemidis, s infelix,而且美國noxia) (p< 0.025),和葡萄球菌(vd: 0.43%, cs: 9.41%;p= 0.000)。這樣,通過CS出生的新生兒胎糞樣品中77.78%(7/9)與vd出生的新生兒胎糞樣品聚類不同,均聚在聚類1中,這是由於上述屬的大量存在(圖S1b).此外,鏈球菌(心絞痛鏈球菌,中間鏈球菌,口腔鏈球菌,美國tigurinus),韋永氏球菌屬(訴atypica而且訴denticariosi),梭狀芽胞杆菌(即。c . histolyticum,c . neonatale而且c . paraputrificum)在cs組(p< 0.035)。
在放線菌門和變形菌門中,有統計學差異的OTUs (p< 0.05)與分娩方式相關,尤其是CS組均較高棒狀杆菌屬。(p< 0.048),腸杆菌屬。(p< 0.02), Erwinia billingiae(p= 0.045),而且Lautropia君子蘭(p= 0.038).
T0時充足孕前BMI與高孕前BMI的比較
在門水平上無統計學差異(圖。3.c),比較孕前體重正常母親(BMI < 25 Kg/m)出生的新生兒胎糞2) vs.懷孕前超重或肥胖的母親(BMI≥25 Kg/m2).
不同的是,在屬水平上,BMI≥25 Kg/m的母親所生的新生兒2的豐度較高鏈球菌(p= 0.026),丙酸菌屬而且放線菌(放線菌;p< 0.04),和Kingella而且Hylemonella(變形菌門;p< 0.045)。在物種層麵上,Alkaliphilus peptidifermentans超重/肥胖母親所生的新生兒高於體重正常母親所生的新生兒(分別為0.78和0.13%;p= 0.016);同樣,在克雷伯氏菌, 3種(k . variicola,k . granulomatis,k .肺炎)的胎糞含量明顯高於體重正常母親所生的胎糞含量(p< 0.023)。
T1時母乳喂養與配方喂養的比較
在門水平上,在配方奶喂養(FF)和母乳喂養(BF)的嬰兒t1 -糞便樣本中也沒有發現統計學差異。3.d)。
排列分析(圖S1D)表明,在統計上不同的屬中(p< 0.05),與bf組相比,配方奶喂養的新生兒腸道菌群相對豐度有較大差異丁酸弧菌屬而且Faecalibacterium(壁厚菌門;p< 0.034),Kitasatospora(放線菌;p= 0.044),Paraprevotella(擬杆菌;p= 0.046),和Trabulsiella(變形菌門;p= 0.02)。與此相反,包括94.12%(32/34)的bf嬰兒糞便樣本的聚類2顯示上述屬的相對豐度為負的歸一化得分。
在物種水平上,有兩種擬杆菌(b . rodentium而且b .均勻化)及兩個Parabacteroides(p . goldsteinii而且p . merdae)均高於BF (p< 0.042)。同樣,在厚壁菌門中,丁酸弧菌屬proteoclasticus,腸球菌casseliflavus而且大腸gallinarum,韋永氏球菌屬atypica而且訴montpellierensisFF (p< 0.05)。在變形菌門中,隻有枸櫞酸杆菌屬werkmanii而且腸杆菌屬aerogenes兩組間差異有統計學意義(p < 0.05)。放線菌種間和小門間差異無統計學意義。
討論
在本研究中,考慮到孕婦孕前BMI (BMI < 25 Kg/m2 vs BMI≥25 Kg/m)等因素,對嬰兒出生時和一個月齡時腸道微生物組組成進行了初步研究2),分娩類型(VD vs CS)和哺乳(母乳喂養vs配方喂養),討論。
結果表明,胎糞中變形菌門(Proteobacteria)在T0時具有較大的優勢,特別是屬於該屬的種埃希氏杆菌屬.先前的研究表明兼性厭氧菌在原始腸道中大量繁殖,從而指向一個相對好氧的腸道環境[19,42].通過這種方式,兼性厭氧菌(如腸杆菌科的成員)找到最佳的生長條件[43],而厚壁菌門、擬杆菌門和放線菌門則在嬰兒期後期占據主導地位[44,45].在我們的研究中也觀察到了相同的腸道微生物環境的演變,與胎糞相比,T1時厚壁菌門的相對豐度顯著增加,而變形菌門和梭菌門的相對豐度顯著降低。
早期生命中的微生物定植受到出生方式的強烈影響,這可能會影響嬰兒出生幾年後的微生物組組成[46].
由VD出生的嬰兒的微生物組組成主要受母體腸道和陰道微生物組的影響,而由CS出生的新生兒的微生物組組成主要受周圍環境的微生物物種(例如醫院環境)和母親的皮膚微生物的影響[17].一些研究已經確定了經陰道分娩和經CS分娩的嬰兒之間存在不同的腸道微生物特征,與經陰道分娩的嬰兒相比,經選擇性CS出生的嬰兒腸道微生物群的豐富度和多樣性較低[17].在我們的樣本中,出生在CS的新生兒表現出更大的兼性需氧菌的相對豐度,如梭狀芽胞杆菌,棒狀杆菌屬,葡萄球菌,鏈球菌可能來源於產婦皮膚、醫院環境或醫院工作人員。此外,一些研究表明,通過CS出生的嬰兒在生命早期觀察到的腸道微生物組組成異常,可能解釋了他們晚年患肥胖症的風險較高[19,42,47].特別是,有人提出,通過CS出生的兒童可能具有更高能力收集食物能量的腸道微生物群,從而使他們容易超重或肥胖[48].
對孕前BMI < 25 Kg/m2和孕前BMI≥25 Kg/m2母親所生新生兒胎糞的微生物組成進行了調查。懷孕前和懷孕期間孕產婦超重與母親和新生兒的不良後果有關;妊娠期肥胖與孕產婦和新生兒發病率增加密切相關,包括妊娠糖尿病、早產、大胎齡嬰兒(LGA)、先兆子癇和先天性異常[49].以往的人體研究表明,懷孕期間超重或肥胖的婦女所生的孩子,在生命的不同階段,腸道微生物組組成存在顯著差異[14,50,51].Collado等人。[14的研究報告顯示,體重超標的母親體內的維生素d含量更高擬杆菌屬在懷孕的最後三個月。高水平的擬杆菌,在孕期超重的婦女中,可能在VD期間垂直傳播給新生兒。事實上,以前的研究報告,在VD新生兒中,革蘭氏陰性菌的相對豐度擬杆菌與體重正常的母親所生的嬰兒相比,超重或肥胖母親所生的嬰兒更容易受到影響[52].相反,有研究表明,孕婦孕前體重指數與糞便中鈣含量呈負相關擬杆菌當嬰兒1個月大時[14].與之前的研究結果相比[14,50,51],在本研究中差異的相對豐度擬杆菌未檢測到sp。需要更多的研究來闡明與母親孕前BMI和分娩方式相關的後代微生物組組成的具體變化。
兩組的主要差異(孕前BMI < 25 Kg/m2和孕前BMI≥25 Kg/m)2)與特定屬和種的相對豐度有關。有趣的是,四分之三的統計上不同的物種屬於克雷伯氏菌在孕前BMI≥25 Kg/m的母親所生的新生兒樣本中較高2.實際上,克雷伯氏菌仍然是醫院感染的主要原因之一,因為經常出現多藥耐藥[53].
在超重或肥胖的受試者中,經常觀察到較高的厚壁菌門水平和較高的厚壁菌門/擬杆菌門比率[54].在厚壁菌門中,我們發現了過度的代表性鏈球菌懷孕前BMI≥25 Kg/m的母親所生的嬰兒2,與cameron Y. Sugino等人最近的研究形成對比。[55].
毫無疑問,隨著時間的推移,對糞便微生物群的評估可能解釋母親孕前BMI如何傳播給嬰兒,以及這將如何影響他們的健康。
喂養類型是觸發早期微生物形成的另一個主要因素,BF和FF嬰兒腸道微生物組成的差異已得到充分證明[54].先前的研究結果顯示,BF嬰兒中雙歧杆菌含量較高,但其多樣性也低於FF嬰兒[56,57].此外,嬰兒早期的微生物組組成主要由母乳喂養嬰兒中參與母乳低聚糖(HMO)代謝的物種所主導[58].這些生物活性化合物似乎對新生兒有益,因為它們不僅能促進更健康的生長,而且還能增強免疫係統,提供預防過敏的保護,還可能提供預防非傳染性疾病(如2型糖尿病、肥胖症)、乳糜瀉、腹瀉和許多其他代謝紊亂的保護[59,60,61,62,63].這就是為什麼世界衛生組織(世衛組織)建議嬰兒在出生後的前6個月應純母乳喂養的主要原因之一[30.].
據先前估計,25-30%的嬰兒細菌微生物群來自母乳,而大約10%來自乳房皮膚的細菌[64].相反,先前的研究表明,嬰兒配方奶喂養的腸道微生物群具有更大的相對豐度特征腸球菌,擬杆菌,Veionella[28,65].與之前的研究相比,我們沒有發現腸微生物組成在門水平上的實質性差異,除了BF嬰兒和FF嬰兒在屬和種水平上的一些例外(圖2)。3.d)。
優勢與局限性
總的來說,A.MA.MI最突出的優勢之一是,從參與者出生一年內獲得的關於母嬰生活方式、終端環境暴露因素的許多方麵的信息具有很大的異質性。問卷調查和結構化訪談中的數據收集和解釋,以及生物樣本的收集和分析以及結果的解釋,需要一個在兒科、臨床營養、微生物學和生物統計學領域具有不同專業知識的多學科團隊的參與。此外,對一些孕前因素的評估,如BMI,證實了產婦體重和生活方式對新生兒微生物群形成的影響。
然而,應該考慮一些局限性。研究人群的樣本量小,時間短,僅涵蓋出生後一年。將考慮擴大隊列和更長時間的隨訪,理想情況下到成年期。最後,計劃隻評估嬰兒微生物群,而不是母親的微生物群。
結論
這些初步和探索性的結果證實,孕前、母嬰因素可能在不同程度上影響嬰兒微生物群組成。特別是,我們發現厚壁菌門相對豐度在一個月後(T1)比胎糞(T0)增加,與變形菌門(Proteobacteria)和梭菌門(Fusobacteria)減少有關。此外,分娩方式(剖宮產vs.陰道分娩)、孕婦孕前BMI (BMI < 25 Kg/m)在屬和種水平上存在顯著差異2vs. BMI≥25 Kg/m2)和根據喂養方式(母乳喂養vs.配方奶喂養)。
這項研究是一項正在進行的縱向前瞻性和觀察性研究,盡管它沒有涵蓋“生命的1000天”,但它有助於目前對孕前、產前和圍產期因素如何影響腸道微生物組組成,從而影響未來宿主健康的理解。此外,所獲得的知識將用於規劃未來的前瞻性觀察隊列,該隊列將在更長時間內進行,旨在識別特定情況的危險因素,並為計劃懷孕的育齡婦女設計量身定製的幹預方案。
數據和材料的可用性
不適用。
縮寫
- 藝術:
-
輔助生殖技術
- 體重指數:
-
身體質量指數
- 剖腹產:
-
剖腹產
- DOHaD:
-
健康與疾病的發展起源
- 全球語言監測機構:
-
廣義線性模型
- 組織:
-
人乳寡糖
- 差:
-
四分位範圍
- 非傳染性疾病:
-
非傳染性疾病
- 辣子雞:
-
操作分類單位
- 主成分分析:
-
主成分分析
- 質量控製:
-
質量控製
- 廁所:
-
腰圍
參考文獻
霍夫曼DJ,雷諾茲RM,哈迪DB。健康和疾病的發展起源:現有知識和潛在機製。生物工程學報,2017;32(12):951-70。
Jacota M, Forhan A, Saldanha-Gomes C, Charles MA, Heude B. EDEN母嬰隊列研究組。EDEN母嬰隊列中母親懷孕前和懷孕期間的體重和後代5-6歲時的BMI和肥胖。兒科醫學雜誌,2017;12(4):320-9。
貝J,雅奎娜D,山田M. DOHaD幹預:青春期和圍孕期的機會。入:薩塔F,福岡H,漢森M,編輯。先發製人的醫學:健康和疾病的發展起源的公共衛生方麵。新加坡:施普林格新加坡;2019.37-51頁。
Mameli C, Mazzantini S, Zuccotti GV。頭1000天的營養:兒童肥胖的起源。中華衛生雜誌。2016;13(9):838。
Cena H, Corvino D, Lops A, Mauri PA, Parazzini F.孕期營養:母親和新生兒的三個關鍵時期。意大利婦產科雜誌,2018;30(2):27-37。
李誌強,李誌強,李誌強,等。腸道菌群組成對慢性非傳染性疾病發病和進展的影響營養。2019;11(5):1073。
Perez-Muñoz ME, Arrieta MC, Ramer-Tait AE, Walter J.“無菌子宮”和“子宮內定植”假設的關鍵評估:對先行者嬰兒微生物組研究的影響。微生物。2017;5(1):48。
Stiemsma LT, Michels KB。微生物組在健康和疾病的發展起源中的作用。兒科。2018;141 (4):e20172437。
Satokari R, Grönroos T, Laitinen K, Salminen S, Isolauri E.人類胎盤中的雙歧杆菌和乳酸杆菌DNA。應用微生物學雜誌,2009;48(1):8-12。
jhnsen FL, Bækkevold ES, Hov JR, Landsverk OJ。長壽的漿細胞能維持腸道內健康的菌群嗎?免疫雜誌2018;39(3):196-208。
Stanislawski MA, Dabelea D, Wagner BD, Sontag MK, Lozupone CA, Eggesbø M.孕前體重,妊娠體重增加,以及母親和嬰兒的腸道微生物群。微生物。2017;5(1):113。
Ajslev TA, Andersen CS, Gamborg M, Sørensen TI, Jess T.腸道菌群建立後兒童超重:分娩方式、孕前體重和早期抗生素給藥的作用。Int J Obes(倫敦)。35 2011;(4): 522 - 29。
Bhagavata Srinivasan SP, Raipuria M, Bahari H, Kaakoush NO, Morris MJ。飲食和運動對母體腸道菌群的影響傳遞給子代。前內分泌(洛桑)。2018; 9:716。
Collado MC, Isolauri E, Laitinen K, Salminen S.母親體重對嬰兒早期微生物群獲取、組成和活性的影響:一項在懷孕早期開始的前瞻性隨訪研究。中華臨床醫學雜誌,2010;29(5):344 - 344。
Vallès Y,弗朗西諾議員。空氣汙染,早期生命微生物群和發育。中國環境衛生研究,2018;5(4):512-21。
Arboleya S, Suárez M, Fernández N, Mantecòn L, Solìs G, Gueimode M,等。剖腹產和新生兒腸道微生物組獲得:對未來健康的影響中國營養學雜誌,2018;73(3):17-23。
Dominguez-Bello MG, Costello E, Contreras M, Magris M, Hidalgo G, Fierer N,等。分娩方式決定了新生兒體內多種身體環境中初始微生物群的獲取和結構。中國科學(d輯:自然科學),2010,26(3):366 - 366。
米勒E,布拉澤M.母乳,配方奶,微生物群和超重。中國內分泌雜誌,2018;14(9):510-1。
Bäckhed F, Roswall J,彭勇,馮強,賈華,Kovatcheva-Datchary P,等。生命第一年人類腸道微生物群的動態和穩定。細胞宿主微生物。2015;17(5):690-703。
Sugino KY, Paneth N, Sarah S. Comstock密歇根隊列確定孕婦孕前體重指數與妊娠和嬰兒胃腸道微生物群落的關係:妊娠晚期和嬰兒早期。PLoS One. 2019;14(3):e0213733。
Galley JD, Bailey M, Kamp Dush C, Schoppe-Sullivan S, Christian LM。母親肥胖與幼兒腸道微生物群的改變有關。公共科學圖書館,2014;9(11):e113026。
Myles IA, Fontecilla NM, Janelsins BM, Vithayathil PJ, Segre JA, Datta SK.父母膳食脂肪攝入量改變子代微生物群和免疫力。中華免疫雜誌,2013;19(6):366 - 366。
馬俊,Prince AL, Bader D, Hu M, Ganu R, Baquero K,等。在靈長類動物模型中,母體懷孕期間的高脂肪飲食會持續改變後代的微生物群。Nat Commun. 2014;5:3889。
Paul HA, Bomhof MR, Vogel HJ, Reiner RA。飲食誘導的母體腸道微生物群和代謝組學變化影響大鼠後代肥胖風險的編程。科學通報2016;6:20683。
Val-Laillet D, Besson M, Guérin S, Coquery N, Randuineau G, Kanzari A,等。在尤卡坦豬的妊娠期和哺乳期,母體的西方飲食可以改變後代的微生物群活性、血脂水平、認知反應和海馬神經發生。王誌強,2017;31:2037-49。
Masukume G, O 'Neill SM, Baker PM, Kenny LC, Morton SMB, khasan AS。剖腹產對兒童超重和肥胖風險的影響:來自當代隊列研究的新證據。科學通報2018;8(1):15113。
妊娠和哺乳期幹擾自身免疫係統對腸道菌群調節的反應。微生物。2019;7(1):105。
王誌剛,王誌剛,王誌剛。母乳喂養和配方奶喂養對新生兒腸道菌群形成的影響。《前端細胞感染微生物》2012;2:94在線發布2012年10月16日。
世衛組織工作人員、世界衛生組織和兒童基金會。2003.
Laursen MF, Bahl MI, Michaelsen KF, Licht TR.第一食品和腸道微生物。《前沿微生物》2017;1:1。
新生兒B組鏈球菌早發性疾病的預防。ACOG委員會意見摘要,第797號。婦產科雜誌2020;135(2):489-92。
Turconi G, Bazzano R, Roggi C, Cena H.意大利成年人定量食物頻率問卷的信度和相對效度。中國食品科學。2010;61(8):846-62。
Craig CL, Marshall AL, Sjöström M, Bauman AE, Booth ML. Ainsworth BE,等國際體育活動問卷:12國信度和效度。中華醫學雜誌。2003;35(8):1381-95。
國際胎兒和新生兒生長聯合會。國際21世紀胎兒和新生兒生長標準(intergrowth -21)研究方案,2009www.intergrowth21.org.uk.
INRAN意大利食品指南,2003年修訂本。http://www.piramidealimentare.it/files_allegati/guida.pdf.
安斯沃思BE, Haskell WL, Whitt MC, Irwin ML, Swartz AM, Strath SJ,等。體育活動綱要:活動規範和MET強度的更新。醫學運動科學雜誌2000;32(增刊9):S498-504。
國家健康和營養檢查調查:人體測量學程序手冊2016https://www.cdc.gov/nchs/data/nhanes/nhanes_03_04/BM.pdf.
Klindworth A, Pruesse E, Schweer T, Peplies J, Quast C, Horn M,等。用於經典和下一代基於測序的多樣性研究的一般16S核糖體RNA基因PCR引物的評估。核酸研究,2013;41(1):1。
阿特舒爾SF,吉什W,米勒W,邁爾斯EW,李普曼DJ。基本的本地對齊搜索工具。中華分子生物學雜誌,1990;215(3):403-10。
Andreotti R, Pérez de León A, Dowd SE, Guerrero FD, Bendele KG, Scoles G.通過標記編碼焦糖測序評估牛蜱根頭菌(Boophilus)的細菌多樣性。BMC微生物學雜誌,2011;11(1):6。
趙海燕,王誌強,王誌強,等。基於隨機豐度模型的物種數量估算。生物識別技術。2002;58(3):531 - 9。
Biasucci G, Rubini M, Riboni S, Morelli L, Bessi E, Retetangos C.分娩方式影響新生兒腸道細菌群落。早期Hum Dev. 2010;86(增刊1):13-5。
Koenig J, Spor A, Scalfone N, Fricker AD, Stombaugh J, Knight R, Angenent LT, Ley RE.發育中的嬰兒腸道微生物群的演代。中國科學院學報(自然科學版)2011;
莊玲,陳宏,張鬆,莊娟,李強,馮哲。早期腸道微生物群及其對兒童健康的影響。基因組學蛋白質組學生物信息,2019;17(1):13-25。
Lorenza P, Federica DC, Andrea P, Pamela V, Bruno D.人類腸道微生物群:與宿主從出生到衰老的動態相互作用。兒科決議2014;76:2-10。
張誌剛,張誌剛,張誌剛,等。影響兒童腸道微生物群的因素:從嬰兒期到兒童期。生物工程學報。2019;44:49。
張誌剛,張誌剛,張誌剛,等。出生方式是否改變了孕婦孕前BMI和妊娠體重增加與嬰兒腸道微生物群的關係?Int J Obes(倫敦)。2020,(1): 44 23-32。
Huh SY, rifasa - shiman SL, Zera CA, Edwards JW, Oken E, Weiss ST, Gillman MW。剖腹產與學齡前兒童肥胖風險:一項前瞻性隊列研究。兒童疾病。2012;97(7):610-6。
米切爾C,查瓦羅JE。分娩方式和兒童肥胖:有值得關注的原因嗎?美國醫學會網絡公開賽。2018;1(7):e185008。
馬培林,王誌強,王誌強,等。陰道分娩是否減輕或加強了超重和肥胖的代際關聯?來自波士頓出生隊列的發現。中國生物醫學工程雜誌,2017;41(4):497-501。
Dutton H, Borengasser SJ, Gaudet LM, Barbour LA, Keely EJ。懷孕期間的肥胖:優化母親和嬰兒的結果。中國臨床醫學雜誌,2018;32(1):344 - 344。
Ley RE, Backhed F, Turnbaugh P, Lozupone CA, Knight RD, Gordon JI。肥胖會改變腸道微生物生態。中國科學院學報(自然科學版)2005;
曹霞,徐霞,張震,沈輝,陳娟,張凱。臨床耐多藥肺炎克雷伯菌分離株的分子特征。臨床微生物學雜誌。2014;13(1):16。
Zacarías MF, Collado MC, Gómez-Gallego C, Flinck H, Aittoniemi J, Isolauri E, Salminen s孕前超重和肥胖與妊娠晚期腸道微生物群組成和全身炎症的差異相關。PLoS One. 2018;13(7):e0200305。
Sugino KY, Paneth N, Comstock SS. Michigan隊列確定孕婦孕前體重指數與妊娠和嬰兒胃腸道微生物群落的關係:妊娠晚期和嬰兒早期。PLoS One. 2019;14(3):e0213733。
casaner O, Goday A, Park YM, Lee SH, Magkos F, Shiow STE, Schröder H.肥胖患者腸道微生物組的係統綜述。國際內分泌雜誌。2018;2018:4095789。
Rodríguez JM, Murphy K, Stanton C, Ross RP, Kober OI, Juge N,等。在整個生命過程中腸道菌群的組成,重點是在生命早期。微生物生態健康雜誌2015;26:26 50。
鄭凱,阮維,金娟。人乳寡糖:腸道菌群的新型調節劑。BMB代表2012;45(8):433-41。
肖l, van 't Land B, van de Worp WRPH, Stahl B, Folkerts G, Garssen J.早期營養因子與自身免疫性糖尿病發展中的粘膜免疫。前麵。Immunol。2017;8:1219。
項WH。母乳喂養、兒童哮喘和過敏性疾病。安。減輕。Metab. 2017;70增刊2:26-36。
Pereira PF, Alfenas Rde CG, Araújo RMA。母乳喂養是否會影響兒童患糖尿病的風險?對現有證據的回顧。中華兒科雜誌2014;90:7-15。
楊曉燕,楊曉燕,Sánchez J,楊曉燕,Picó C.母乳瘦素在發育中嬰兒體重控製中的作用。肥胖。2006;14:1371-7。
de Palma G, Capilla A, Nova E, Castillejo G, Varea V, Pozo T, Sanz Y.母乳喂養類型和乳糜瀉遺傳風險對嬰兒腸道微生物群的影響:PROFICEL研究科學通報。2012;7:e30791。
ststrand TA, Sharma PR, Gjessing HK, Ulak M, Chandyo RK, Adhikari RK, Sommerfelt H.嬰幼兒急性腹瀉持續時間延長的危險因素。PLoS ONE。2012; 7: e36436。
Pannaraj PS, Li F, Cerini C, Bender JM, Yang S, Rollie A,等。母乳細菌群落與嬰兒腸道微生物群的建立和發展之間的聯係。美國兒科雜誌,2017;171:647-54。
確認
我們感謝Umberto Veronesi基金會為Benedetta Raspini博士提供“2019年博士後獎學金”研究資助。我們也要熱烈感謝Andrea Quadrelli先生和Elettra Cesare女士在招收二元組(問卷和訪談管理、樣本收集和數據輸入)方麵的幫助;感謝Micol Angelini博士和Andrea Frontini教授在樣品收集和儲存方麵的幫助;感謝所有護理人員在招聘和跟進階段的幫助和合作。
資金
本研究尚未獲得任何資助。
作者信息
作者及隸屬關係
貢獻
BR和DP在研究的概念和設計、結果解釋和起草手稿方麵均有貢獻;RDG和MC對研究的概念、設計、結果解釋和審稿做出了貢獻;RMC、EC和FG對研究的概念和設計做出了貢獻;CM進行統計分析並對稿件進行修改;MDA進行統計分析,解釋結果並修改稿件;HC起草、修改並批準最終稿。所有作者都已閱讀並批準了本版本的手稿,並聲明該內容未在其他地方發表過。
相應的作者
道德聲明
倫理批準並同意參與
該研究得到了帕維亞基金會(Fondazione IRCCS Policlinico S. Matteo)人類倫理委員會的批準(協議號:20180022618;2018年6月12日),並將根據良好臨床實踐指南進行。
發表同意書
我們會提供家長/合法監護人的書麵知情同意。帕維亞的IRCCS Policlinico S. Matteo基金會的人類倫理委員會批準了這一程序。
相互競爭的利益
作者宣稱他們之間沒有利益衝突。
額外的信息
出版商的注意
beplay外围下载施普林格自然對出版的地圖和機構從屬關係中的管轄權主張保持中立。
補充信息
附加文件1:表S1
.在胎糞(T0)和新生兒1個月(T1)後的糞便樣本中發現的Reads通過過濾質量的數量、Reads分類到屬級的百分比、Shannon多樣性指數和鑒定物種(OTUs)的平均值:A);B)在剖宮產(CS)或陰道分娩(VD)出生的新生兒胎糞中;C)在出生體重正常(BMI < 25 Kg/m)的新生兒胎糞中2)超重或肥胖的母親(BMI≥25 Kg/m2))和D)在t1 -以配方奶喂養(FF)或母乳喂養(BF)的新生兒樣本中。
附加文件2:圖S1a。
排列分析總結相對豐度> 0.1%的屬,差異有統計學意義(p值< 0.05;學生t檢驗),在新生兒(T0)和1月齡後(T1)胎糞中發現。圖印地。陰道分娩(VD)和剖宮產(CS;在紅框中突出顯示)。圖就是S1c。排列分析總結相對豐度> 0.1%的屬,差異有統計學意義(p-value< 0.05),在出生體重正常(BMI < 25 Kg/m)的新生兒胎糞中發現2)或超重或肥胖(BMI≥25 Kg/m)的母親2;在紅框中突出顯示)。圖S1d。排列分析總結相對豐度> 0.1%的屬,差異有統計學意義(p-value< 0.05),在母乳(BF)或配方奶(FF;在紅框中突出顯示)。
附加文件3:圖S2a
.排列分析總結相對豐度> 0.1%的物種,差異有統計學意義(p值< 0.05;學生t檢驗),在新生兒(T0)和1月齡後(T1)胎糞中發現。圖開通.排列分析總結相對豐度> 0.1%的種,差異有統計學意義(p值< 0.05;學生t檢驗),在陰道分娩(VD)或剖宮產(CS;在紅框中突出顯示)。圖S2c。排列分析總結相對豐度> 0.1%的種,差異有統計學意義(p值< 0.05;學生t檢驗),在正常體重(BMI < 25)或超重/肥胖母親(BMI≥25;在紅框中突出顯示)。圖S2d.排列分析總結相對豐度> 0.1%的種,差異有統計學意義(p值< 0.05;在用母乳(BF)或配方奶(FF;在紅框中突出顯示)。
權利和權限
開放獲取本文遵循知識共享署名4.0國際許可協議,允許以任何媒介或格式使用、分享、改編、分發和複製,隻要您對原作者和來源給予適當的署名,提供知識共享許可協議的鏈接,並注明是否有更改。本文中的圖像或其他第三方材料包含在文章的創作共用許可協議中,除非在材料的信用額度中另有說明。如果材料未包含在文章的創作共用許可協議中,並且您的預期使用不被法定法規所允許或超出了允許的使用範圍,您將需要直接獲得版權所有者的許可。如欲查看本牌照的副本,請瀏覽http://creativecommons.org/licenses/by/4.0/.創作共用公共領域奉獻棄權書(http://creativecommons.org/publicdomain/zero/1.0/)適用於本條所提供的資料,除非在資料的信用額度中另有說明。
關於本文
引用本文
Raspini, B., Porri, D., De Giuseppe, R.。et al。產前和產後決定因素塑造後代的微生物組在前1000天:研究方案和初步結果在一個月的生命。兒科J醫院46, 45(2020)。https://doi.org/10.1186/s13052-020-0794-8
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-020-0794-8
關鍵字
- 腸道微生物群
- 懷孕
- 交貨方式
- 母乳喂養
- 妊娠暴露因素
- 健康和疾病的發展起源(DOHaD)