- 研究
- 開放獲取
- 發表:
生長激素生物仿製藥Omnitrope®在需要生長激素治療的兒童中的長期安全性和有效性:意大利PATRO兒童研究的中期分析
beplay怎么下载安装體積42,文章號:93(2016)
摘要
背景
PATRO Children是一項持續的觀察性、縱向、非介入性、全球上市後監測研究,旨在調查Omnitrope®(一種與Genotropin®類似的生長激素生物仿製藥)在生長障礙兒童中的長期安全性和有效性。PATRO兒童的主要終點是長期安全性,次要終點是有效性,通過分析身高(HSDS)和身高速度(HVSDS)標準差評分等輔助學數據進行評估。在這裏,我們報告了截至2015年8月的意大利PATRO兒童數據的中期分析數據。
方法
PATRO兒童正在招募被診斷患有矮小疾病需要GH治療並正在接受Omnitrope®的兒童。在所有Omnitrope®治療的患者中評估不良事件(AEs)。身高每年評估接近成年(最終)身高,並在此報告為HSDS;高度速度也評估和報告為標準偏差評分(HVSDS)。
結果
截至2015年8月,共納入186例患者(平均年齡10.2歲,57.5%為男性):156例[84%]生長激素缺乏,12例[6.5%]出生時小於胎齡,7例[3.8%]prard - willi綜合征,1例[0.5%]Turner綜合征,1例[0.5%]慢性腎功能不全;7例(3.8%)患者有其他適應症。Omnitrope®的平均治療時間為28.1±19.1個月。35.6%的患者報告了不良事件,包括頭痛、發熱、關節痛、腹痛、腿和/或手臂痛以及血磷酸肌酸激酶升高。2例患者中2例嚴重ae被認為與藥物有關;一名患者經曆了已知殘留顱咽管瘤的微小增加,另一名患者伴有行走困難惡化的步態障礙。與研究性研究類似,Omnitrope®治療與HSDS和HVSDS的改善相關。
結論
Omnitrope®似乎對廣泛的兒科適應症具有良好的耐受性和有效的治療,這與對照臨床試驗的結果一致。在全球PATRO兒童研究的數據可用之前,需要謹慎地解釋這些結果。
背景
在過去的30年裏,幾種重組人類生長激素(rhGH)產品已被批準用於治療與身材矮小相關的生長障礙兒童[1- - - - - -7],多項觀察性和隨機性研究均證實了rhGH產品(也稱為生長激素)的有效性和安全性[8- - - - - -12].
Omnitrope®(山德士,昆德爾,奧地利),由轉化菌株表達大腸杆菌gentropin(輝瑞有限公司,Sandwich,英國)作為生物仿製藥研發,2006年成為首個通過歐洲生物仿製藥監管途徑獲得歐洲藥品管理局(EMA)批準的產品。Omnitrope®已獲許可用於治療生長激素缺乏(GHD)兒童,以及那些可能影響生長的疾病,如特納綜合征(TS)、慢性腎功能不全(CRI)、prard - willi綜合征(PWS)和出生時小於胎齡的兒童(SGA) [13].
Omnitrope®的關鍵III期研究結果表明,Omnitrope®對患有GHD的嬰兒、兒童和青少年是安全有效的。9,14];然而,需要更多Omnitrope®在兒科患者中的真實數據來鞏固臨床實踐中的III期結果。為了解決這一問題,啟動了全硝繩治療的患者(PATRO)兒童研究。PATRO Children是一項長期上市後監測(PMS)研究,旨在調查Omnitrope®對生長障礙兒童的安全性和有效性。這是Omnitrope®風險管理計劃的一部分,以履行對EMA的承諾。本研究納入的患者截至2012年9月的1年中期結果(n= 1837)之前已經報道過[15],並在國際會議上提交年度最新情況[16].截至2016年1月,PATRO兒童研究從14個國家(奧地利、捷克共和國、法國、德國、意大利、波蘭、羅馬尼亞、斯洛文尼亞、西班牙、瑞典、台灣、英國、加拿大和美國)的291個地點招募了4675名患者。在此,我們介紹了在意大利17個地點招募的186名患者的結果,代表了自研究開始至2015年8月在意大利招募的患者亞組。
方法
研究設計
這項多中心、開放、縱向、非介入性經前症候群研究的設計已在以前詳細發表[15].簡而言之,本研究在Omnitrope®獲批的幾個國家的兒童醫院和專業內分泌科診所進行。參與研究的患者為接受Omnitrope®治療的嬰兒、兒童和青少年,並獲得父母或法定監護人的書麵知情同意。Hormone-naïve患者和以前接受過rhGH的患者都符合納入條件。該研究由每個研究地點的獨立倫理委員會/機構審查委員會審查和批準,並根據《奧維耶多人權公約》和《赫爾辛基宣言》進行。
治療和結果
PATRO兒童研究中納入的患者根據產品特性摘要中的建議接受了Omnitrope®治療[13]及/或有關國家的處方資料。這項正在進行的觀察性研究的主要目的是收集和分析在常規臨床實踐中治療的嬰兒、兒童和青少年Omnitrope®的長期安全性數據,特別強調以下方麵:在出生在SGA並因生長障礙而治療的兒童中,rhGH治療的糖尿病發生潛力,rhGH治療的患者中惡性腫瘤的發生,抗rhGH抗體的發生和臨床意義以及PWS患者中rhGH治療的風險。
所有不良事件(AEs)、嚴重不良事件(sae)、藥物不良反應(adr)和嚴重不良反應均記錄在電子病例報告表格中,並輸入山德士安全數據庫。在研究期間,至少每年記錄一次實驗室值(包括葡萄糖代謝)。
次要目標是收集和分析治療效果的數據。療效終點包括源自身高測量的自體數據身高標準差評分(HSDS)和身高速度標準差評分(HVSDS) [17,18].
統計分析
在此中期分析中,使用SAS版本9.3軟件包進行統計計算。AEs使用監管活動醫學詞典(MedDRA) 17.1版進行編碼。伴隨用藥根據世界衛生組織藥物詞典(14.3版)進行編碼,用藥按當前版本的解剖治療化學術語進行表列。對於連續/定量變量,計算描述性統計,包括可用數據值的數量,缺失數據值的數量,算術平均值,標準差,最小值,中位數和最大值。在適當的情況下,連續參數進行比較t-檢驗或Wilcoxon非參數檢驗。對於分類/定性變量,編製了頻率表和百分比表。適當時,使用卡方檢驗或Fisher精確檢驗對分類數據進行比較。統計學檢驗為雙側,顯著性水平為0.05。
結果
截至2015年8月,意大利17個地點共納入186例患者,平均年齡10.2歲,其中57.5%為男性(表2)1)並接受Omnitrope®治療,平均28.3±19.1個月。大部分病人(n= 156;84.0%)為GHD, 12例(5.6%)為SGA, 7例(3.8%)為PWS, 1例(0.5%)為CRI, 1例(0.5%)為TS;7例(3.8%)患者納入了其他適應症資料。總體而言,89.8%的患者naïve接受激素治療,Omnitrope®是他們的第一種治療方案。其餘患者(10.2%)所有適應症的平均生長激素治療前持續時間(27.8±19.2個月)相似,隻有一名PWS患者的治療前持續時間為47.3個月。
在本分析時,85例患者在PATRO兒童研究中已停止記錄。停藥原因包括:患者達到最終身高/骨齡成熟(n= 26;30.6%);改用其他生長激素產品(n= 21;24.7%;這些患者都來自一個站點,在決定中斷數據生成後,於2011年11月至2012年1月期間切換到其他rhGHs);無法跟進(n= 7;8.2%);其他原因(n= 6;7.1%);AEs (n= 2;2.4%);高度速度減慢至每年1厘米以下(n= 1;1.2%);患者不願繼續注射(n= 1;1.2%)和患者不服從(n= 1;1.2%)。其餘20例患者(23.5%)停藥原因不明。
安全
截至2015年8月,意大利安全性分析集中納入的186例患者中,有66例(35.6%)在數據庫中登記了142例ae。報告的最常見ae(發生率> 9.12 / 438.8患者-年)為頭痛(13例;7.0%;GHDn= 12,其他n= 1)、發熱(7例;3.8%;GHDn= 5, sgan= 1, crin= 1)、關節痛(5例;2.7%;GHDn= 5)、腹痛(4例;2.2%;GHDn= 2, sgan= 1,其他n= 1),腿和/或手臂疼痛(4例;2.2%;GHDn= 3,其他n= 1),血磷酸肌酸激酶升高(4例;2.2%;GHDn= 4)。18例(9.1%)患者發生19例adr;一位患者經曆兩次磷酸肌酸激酶水平升高。可用MedDRA首選術語的adr數量為17(發病率> 2.28);這些總結在表中2.在GHD患者中報告了另外兩個沒有MedDRA首選條款的adr;1例男性患者亞臨床甲亢,1例女性患者胰島素樣生長因子-1 (IGF-1)高(667.4 ng/mL)。
8例(4.3%)患者共發生10例急性呼吸道綜合征。其中,2例GHD患者的2例sae被認為可能與Omnitrope®治療有關。一名既往患有顱咽管瘤的患者(19歲男性)在使用Omnitrope®5年後,殘餘顱咽管瘤的大小略有增加。出於安全原因,Omnitrope®在該患者中停用,4個月後重新啟動;由於隨後的磁共振成像(MRI)掃描沒有證實這種增加,因此該事件被報告為完全解決。第二例患者(一名8歲男性)患有骨骼發育不良和並指畸形,伴有步態障礙,行走困難惡化。在該患者中,Omnitrope®治療被永久停用,該事件的結果未被報道。
迄今為止,使用Omnitrope®治療的1型或2型糖尿病尚未確診病例;然而,2例患者有輕度糖耐量受損。與全球初步結果相似,沒有生長激素相關惡性腫瘤或研究者報告的抗rhgh抗體滴度數據的報道。在PWS患者中,2例患者報告了4例ae;第一個患者有一個輕度AE(支氣管炎)和兩個sae(肺不張,間質性肺疾病),而第二個患者有睡眠呼吸暫停綜合征,被認為與藥物有關。
功效
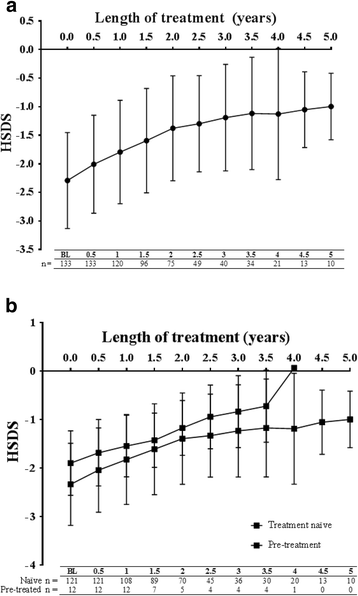
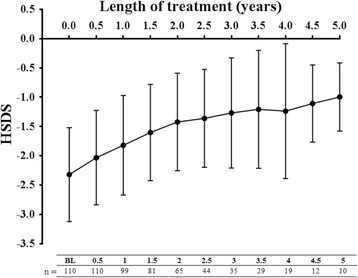
Omnitrope®治療後,HSDS值在總患者人群中隨著時間的推移逐漸改善(圖2)。1),由平均HSDS值-2.29±0.84 (n= 133)在基線至-1.13±1.15 (n= 4年級。這種正向趨勢持續到第5年(-0.10±0.58 [n= 10]),無論治療前狀態如何,HSDS均有改善(圖10)。1 b).在hormone-naïve GHD患者中觀察到類似的趨勢(圖。2).由於少數意大利患者有GHD以外的適應症,所獲得的數據在統計學上沒有意義。
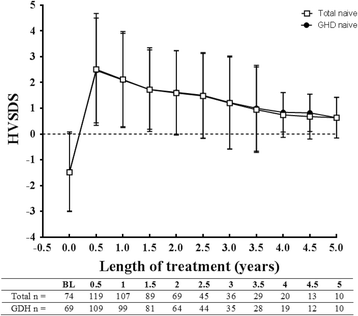
在hormone-naïve例患者中,平均HVSDS從基線值-1.49±1.50 (n= 74),至0.5年峰值均值2.50±2.17 (n= 119), 4.0歲時穩定在0.74±0.87 (n= 20), 5.0歲為0.63±0.79 (n= 10;無花果。3.).在hormone-naïve GHD患者中也觀察到HVSDS的這種趨勢。3.)和出生時SGA(從-1.79±0.82 [n= 4]至1.5歲時的1.13±1.23 [n= 4])。
討論
中期分析結果顯示,Omnitrope對需要rhGH治療的生長障礙意大利兒童具有良好的耐受性和有效性。最常見的不良事件報告為頭痛、發熱、關節痛、腹痛和血磷酸肌酸激酶升高。9.1%的患者報告有不良反應,其中2例被認為是嚴重的。
一些研究表明,rhGH治療與糖尿病的發展之間存在聯係[19],而其他研究並沒有建立同樣的關係[9,20.].更具體地說,SGA出生的兒童可能會增加患胰島素抵抗和2型糖尿病的風險[21人們擔心rhGH可能會放大這一風險。一項基於Kabi Pharmacia國際生長研究(KIGS)數據庫的研究評估了rhGH治療對PWS患兒的不良事件,報告稱4例患者出現高血糖,6例患者在治療後推定患有糖尿病[22].根據我們的研究結果,在沒有1型或2型糖尿病病例報告的情況下,Omnitrope®III期臨床研究的結果,以及全球PATRO兒童研究發表的第一個數據,不支持rhGH治療與糖尿病之間的聯係[14,15];然而,rhGH治療與糖尿病發展之間的潛在聯係仍需在日常臨床實踐中得到證實。
關於rhGH治療與癌症風險之間是否存在關聯,有相互矛盾的證據[23].觀察發現,生長激素可以提高IGF-1的血清濃度,因為IGF-1具有有絲分裂和抗凋亡的特性在體外在動物模型中也是如此[24].在接受生長激素治療的癌症患者中,與未接受治療的癌症患者相比,癌症的發生以及發生第二種惡性腫瘤的風險增加[24].然而,一項基於KIGS數據庫的研究報告稱,rhGH治療與癌症發病率增加之間沒有關聯[25].在意大利PATRO兒童研究數據的中期分析中,一名患者出現殘留顱咽管瘤增加,治療暫時中斷,盡管隨後的MRI掃描沒有證實這種增加。為了進一步調查中期分析中惡性腫瘤的發生率,需要將這些發現與全球PATRO兒童研究的結果進行比較。無其他疑似與Omnitrope®治療相關的惡性腫瘤報道,在數據截止時,沒有研究者報告的抗rhgh抗體滴度。
療效數據表明Omnitrope®對意大利兒科患者的生長參數有積極影響,證實了III期試驗的結果。與研究性研究類似,Omnitrope®治療可改善GHD患兒的HSDS和HVSDS [9,14].正如預期的那樣,接受了rhGH預處理的患者的基線HSDS高於rhGH naïve的患者,但兩個人群的反應遵循相同的趨勢。
一項基於KIGS數據庫的研究報告了在接受rhGH替代治療後,白人GHD患者的中位HSDS從男性的-2.4到-0.8,女性的中位HSDS從-2.6到-1.0 [26].這些結果與本研究報告的結果相似,但由於治療持續時間和基線年齡的差異,很難進行比較。事實上,對KIGS數據庫的分析已經證實了治療開始時的年齡與生長反應之間的負相關[26].
該分析結果與截至2012年9月的全球PATRO兒童研究報告一致[15].這些來自PATRO兒童研究的數據支持Omnitrope®在常規臨床實踐中具有良好的耐受性;沒有糖尿病確診病例,沒有惡性腫瘤的報道,也沒有其他安全問題的報道。然而,考慮到2015年8月的截止日期,PATRO兒童研究的完整分析中包括的患者的特征與目前對意大利患者的分析之間存在一些差異。在全球分析中,58.7%的患者為GHD, 25.9%的患者為先天性SGA,其餘兒童診斷為TS(4.4%)、PWS(2.3%)、CRI(0.7%)或其他診斷(6.0%)[15].相比之下,在意大利的分析中,GHD患者的比例非常高(約80%的患者),而隻有6.5%的患者出生時為SGA。這可能表明,與其他國家相比,意大利兒童的診斷和/或治療方式有所不同。
這項分析的結果也與PATRO兒童研究的整體最新數據一致,該研究於2016年1月進行了分析(數據存檔)。在迄今為止招募的4675例患者中,Omnitrope®治療的平均持續時間為30.2±22.0個月。總體而言,1653例(35.4%)患者經曆了ae, 248例(5.3%)患者經曆了SAE;22例(0.5%)患者被認為與治療相關。1例逐漸發病的1型糖尿病已被報道,沒有rhgh相關惡性腫瘤或其他安全問題的報道。此外,尚無臨床相關的抗rhgh抗體滴度陽性報道。療效數據表明,Omnitrope®對兒童生長參數有積極影響:4年治療後,Omnitrope®在所有適應症的生長參數上均有顯著改善,無論性別或治療前狀態如何。特別是,在治療的頭4年裏,hormone-naïve患者觀察到更高的身高增長,平均HVSDS (SD)為1.66 (2.67),GHD患者為ΔHVSDS +4.56 (n= 411)和0.80(2.21)和ΔHVSDS +3.41(出生時SGA (n= 231)。
PWS是一種罕見的疾病,PATRO兒童研究為調查PWS兒童對rhGH治療的反應提供了機會[15].在對意大利患者的中期分析中,一名患者報告輕度睡眠呼吸暫停綜合征,被認為與rhGH治療有關。在一項基於KIGS數據庫的研究中,睡眠呼吸暫停被報道為一名接受生長激素治療的PWS患者的死亡原因[22].雖然rhGH治療在意大利PWS患兒的總體人群中似乎具有相對較好的耐受性,但由於患者人數較少,因此需要謹慎解釋這些結果(n= 7),並需要PATRO兒童研究的全球分析來證實。
雖然該分析結果支持Omnitrope®的長期介入試驗,但這些結果的解釋存在一些局限性。本分析中納入的患者主要診斷為GHD,如前所述,在所有不同的rhGH治療適應症中,這並不能代表治療結果。然而,我們認為這項研究反映了意大利的真實臨床實踐,可以這樣解釋。
結論
該分析表明,Omnitrope®在常規臨床實踐中對廣泛的兒科適應症具有良好的耐受性和有效。生長激素生物仿製藥Omnitrope®的安全性和有效性與對照臨床試驗中觀察到的一致。所有這些數據都有助於排除在現實臨床實踐中使用生物仿製藥的假定性擔憂。
縮寫
- 美國存托憑證:
-
藥物不良反應
- AE:
-
不良事件
- 中國國際廣播電台:
-
慢性腎功能不全
- 教育津貼:
-
歐洲藥品管理局
- GHD:
-
生長激素缺乏
- hsd:
-
高度標準差得分
- HVSDS:
-
高度速度標準偏差得分
- igf - 1:
-
胰島素樣生長因子-1
- KIGS:
-
卡比法瑪西亞國際成長研究
- 核磁共振成像:
-
磁共振成像
- PATRO:
-
Omnitrope®治療的患者
- 項目經理:
-
上市後監測
- 漿:
-
二氏綜合征
- rhGH:
-
重組人生長激素
- 薩德爾:
-
嚴重藥物不良反應
- SAE:
-
嚴重不良事件
- SGA:
-
對於胎齡來說太小了
- TS:
-
特納綜合征
參考文獻
Cook DM, Yuen KC, Biller BM, Kemp SF, Vance ML.美國臨床內分泌學家協會生長激素缺乏成人和過渡患者臨床應用醫學指南- 2009年更新:建議執行摘要。中國醫藥科學。2009;15(6):580-6。
生長激素研究學會。診斷和治療兒童和青少年生長激素(GH)缺乏症的共識指南:生長激素研究學會的總結聲明。中國臨床內分泌雜誌,2000;29(4):489 - 497。
Clayton PE, Cuneo RC, Juul A, Monson JP, Shalet SM, Tauber M.關於在向成人護理過渡中接受gh治療的青少年管理的共識聲明。中華內分泌雜誌,2005;29(2):344 - 344。
特納綜合征女童和婦女的護理:特納綜合征研究小組的指導方針。中國臨床內分泌雜誌,2007;29(1):10-25。
Lee PA, Chernausek SD, Hokken-Koelega AC, Czernichow P.國際小胎齡谘詢委員會共識發展會議聲明:管理小胎齡出生的矮個子兒童,2001年4月24日至10月1日。兒科學。2003;111(6 Pt 1): 1253-61。
馬漢JD, Warady BA。慢性腎病兒童患者身材矮小的評估和治療:一項共識聲明兒科腎內科雜誌。2006;21(7):917-30。
Goldstone AP, Holland AJ, Hauffa BP, Hokken-Koelega AC, Tauber M. prard - willi綜合征的診斷和治療建議。中國臨床內分泌雜誌,2008;29(11):483 - 483。
羅默,李誌強,李誌強,李誌強,等。一種新的即食重組人生長激素溶液的有效性和安全性。中華內分泌雜誌。2007;30(7):578-89。
López-Siguero J, Borras Perez MV, Balser S, Khan-Boluki J.重組人生長激素Omnitrope®治療西班牙生長激素缺乏兒童的長期安全性和有效性:一項III期研究的結果。獸醫學報,2011;28(10):879-93。
金勇,洪繼偉,鄭玉生,金文文,趙耀文,金誌華,等。緩釋重組人生長激素對韓國成人生長激素缺乏症的療效和安全性。延世醫學雜誌,2014;42(4):1042-8。
Tabatabaei-Malazy O, Mohajeri-Tehrani MR, Heshmat R, Taheri E, Shafiee G, Razzaghy-Azar M,等。薩姆托平重組人生長激素的療效和安全性雙盲隨機臨床試驗。中華糖尿病雜誌。2014;13(1):115。
Borrás Pérez V, López-Siguero JP, Martínez G, Corripio R, Fernández JM, Labarta JI,等。一項監測西班牙生長激素缺乏症兒童成年身高的隨訪研究,這些兒童在III期臨床試驗期間接受了生物仿製藥人重組生長激素(Omnitrope®)。中華獸醫雜誌,2015;32(2):148-56。
歐洲藥品管理局。Omnitrope®產品特性總結。2015.可從URL:http://www.ema.europa.eu/docs/en_GB/document_library/EPAR_-_Product_Information/human/000607/WC500043695.pdf.2015年11月19日訪問。
羅默T, senger P, Peter F, Walczak M, Le Bouc Y, Khan-Boluki J,等。重組人生長激素全硝索治療生長激素缺乏兒童7年的安全性和有效性:III期研究結果中國科學,2009;29(6):359-69。
Pfäffle R, Schwab KO, Marginean O, Walczak M, Szalecki M, Schuck E,等。PATRO Children是一項多中心、非介入性研究,研究Omnitrope®在需要生長激素治療的兒童中的長期療效和安全性。中國內分泌雜誌,2013;4(1):3-11。
Pfäffle R, Kanumakala S, Hoybye C, Kristrom B, Schuck E, Zabransky M,等。截至2015年1月,PATRO Children是一項多中心、非介入性研究,研究Omnitrope®在需要GH治療的兒童中的長期安全性和有效性。《兒科雜誌》2015;84增刊1:42 - 8。
李誌強,李誌強,李誌強,等。新生兒人體測量圖:意大利新生兒研究與其他歐洲研究的比較。中華兒科胃腸病學雜誌,2010;51(3):353-61。
Tanner JM, Whitehouse RH。身高、體重、身高速度、體重速度和青春期階段的臨床縱向標準。阿奇迪斯兒童。1976;51(3):170-9。
Cutfield WS, Wilton P, Bennmarker H, Albertsson-Wikland K, Chatelain P, Ranke MB,等。接受生長激素治療的兒童和青少年中糖尿病和糖耐量受損的發生率。柳葉刀》。2000;355(9204):610 - 3。
Allen DB, Backeljauw P, Bidlingmaier M, Biller BM, Boguszewski M, Burman P,等。生長激素安全車間立場文件:兒童和成人重組人生長激素治療的關鍵評估。中華內分泌雜誌,2015;29(2):344 - 344。
Boyko EJ。胎兒生長受損導致2型糖尿病病例的比例。糖尿病護理。2000;23(9):1260-4。
Craig ME, Cowell CT, Larsson P, Zipf WB, Reiter EO, Albertsson Wikland K,等。Prader-Willi綜合征的生長激素治療和不良事件:數據來自KIGS(輝瑞國際生長數據庫)。臨床內分泌(Oxf)。2006, 65(2): 178 - 85。
蔡華威,金德華,金海生。生長激素治療與惡性腫瘤的風險。中華兒科雜誌,2015;58(2):41-6。
Swerdlow AJ。生長激素療法會增加患癌症的風險嗎?中華實用內分泌雜誌。2006;2(10):530-1。
Wilton P, Mattsson AF, Darendeliler F.兒童生長激素治療與癌症發病率增加無關:來自KIGS(輝瑞國際生長數據庫)的經驗中華兒科雜誌,2010;157(2):265-70。
Reiter EO, Price DA, Wilton P, albertson - wikland K, Ranke MB.生長激素治療對1258例特發性生長激素缺乏患者近終身高的影響:一個大型國際數據庫的分析。中國臨床內分泌雜誌。2006;91(6):2047-54。
致謝
起草大綱和初稿的醫學寫作協助由Simone Boniface和Cécile Duchesnes博士提供,施普林格醫療保健通信。這項醫學寫作援助由意大利山德士公司資助。
我們還要感謝巴裏大學的Luciano Cavallo教授,意大利Troina Oasi Maria SS的Benedetta Moscuzza博士,以及參與這項研究的CRO MAPI小組,特別是Stefania Lamartina, Diletta Ippolito和Giovanna Sabatini。
資金
這項研究由山德士公司資助。
數據和材料的可用性
PATRO兒童數據庫並非免費提供。
作者的貢獻
所有作者都參與了招募研究患者、進行內分泌評估和數據采集、修改/批準稿件。
相互競爭的利益
MES一直擔任山德士的顧問,並參與主辦的會議;國民陣線和自由人民黨從山德士公司獲得讚助大會的補償;EZ和AP是山德士公司的雇員;所有其他作者都聲明沒有利益衝突。
發表同意書
不適用。
倫理批準並同意參與
在研究開始前,該研究由每個研究地點的獨立倫理委員會或機構審查委員會審查和批準。這項研究是根據《奧維耶多人權公約》和《赫爾辛基宣言》進行的。該研究招募了正在接受Omnitrope®治療並獲得父母或法定監護人書麵知情同意的嬰兒、兒童和青少年。
作者信息
作者及隸屬關係
相應的作者
權利和權限
開放獲取本文根據創作共用屬性4.0國際許可協議(http://creativecommons.org/licenses/by/4.0/),允許在任何媒介上不受限製地使用、分發和複製,前提是您對原作者和來源給予適當的讚揚,提供到創作共用許可證的鏈接,並注明是否進行了更改。創作共用公共領域奉獻棄權書(http://creativecommons.org/publicdomain/zero/1.0/)除另有說明外,適用於本條所提供的資料。
關於本文
引用本文
尤蓋蒂,L,托內斯,G,史崔特,法醫et al。生長激素生物仿製藥Omnitrope®在需要生長激素治療的兒童中的長期安全性和有效性:意大利PATRO兒童研究的中期分析兒科J醫院42, 93(2016)。https://doi.org/10.1186/s13052-016-0302-3
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-016-0302-3
關鍵字
- 青少年
- 孩子們
- 嬰兒
- Omnitrope®
- 兒科
- 重組人生長激素