摘要
背景
新生兒21羥化酶缺乏症篩查旨在檢測經典形式的先天性腎上腺增生(CAH)。目前尚不清楚在新生兒篩查中出現假陽性的新生兒是否會在以後出現雄激素過量的跡象。本研究的目的是驗證新生兒篩查中17-OHP的輕微升高是否為早熟的預測因素。
方法
我們評估了2001年至2014年出生的所有早產嬰兒。如果骨骼年齡增加,他們將接受功能測試,以找出症狀的原因。重新考慮了他們在新生兒CAH篩查中的17-OHP值。
結果
我們確定了330例(269名女性,61名男性)陰部過早的患者。所有這些兒童在新生兒篩查時的17-OHP均正常,除了一名早產且未受CAH影響的兒童。
結論
新生兒篩查中17-OHP升高並不是早產的預測因素。篩查時17-OHP水平升高的一個可能原因是腎上腺發育不成熟或新生兒應激。因此,在兒童時期對這些新生兒進行嚴格的隨訪是不必要的。
背景
自2001年以來,在意大利東北部建立了先天性腎上腺增生(CAH)新生兒篩查項目,該項目基於對濾紙幹燥的血點進行17-羥孕酮(17-OHP)檢測。該研究旨在早期鑒定受典型形式21羥化酶缺乏症(21- ohd)影響的新生兒,從而預防因鹽浪費引起的潛在危及生命的休克,特別是男性新生兒,以及受影響的女孩因不適當的男權化而發生的不正確性別分配[1,2,3.,4].然而,這種新生兒篩查的真正可持續性仍然存在爭議。事實上,一些研究強調了新生兒篩查決定的高回憶率,特別是在早產兒中,並指出了導致這些回憶的心理和經濟成本,這需要去看兒科醫生和血清確認性測試[5,6].為了防止這些缺陷,我們之前曾建議避免對CAH新生兒篩查結果呈陽性且不存在經典形式CAH的新生兒進行進一步研究,當出生後血清17-OHP水平隨時間下降時[7].然而,篩查程序不能識別非典型21-OHD的嬰兒,因為這種類型的疾病患者的基礎血清17-OHP水平通常在正常範圍內[1,8,9,10,11].因此,如果出現進一步的症狀,如陰部過早、痤瘡、多毛症,建議進行其他更具體的確認性評估,即功能測試[1,3.,7].事實上,目前尚不清楚新生兒篩查中17OHP水平略高的新生兒是否會在以後出現陰部過早或雄激素過量的其他症狀。此外,過早識別早熟陰部是有用的,因為它可以減少相關並發症,如肥胖和胰島素抵抗[12,13].
因此,本研究的目的是驗證新生兒篩查中17-OHP升高是否為早熟的預測因素。
方法
我們在這項研究中招募了2001年至2014年間出生的所有嬰兒,這些嬰兒後來被轉診到意大利維羅納醫院的兒科內分泌科,因為過早的陰毛被定義為女孩在8歲之前或男孩在9歲之前出現陰毛。
采用Tanner和Whitehouse方法對所有患者進行評估,以確定他們的體重、身高、BMI和青春期發育[14].對於男孩,使用普拉德睾丸量計評估睾丸體積。所有兒童均接受x線攝影以確定骨年齡,並采用Greulich和Pyle方法評估[15].在高齡骨齡兒童中,進行血液測試以測量血清17-OHP,皮質醇,睾酮,ACTH, DHEAS, Δ4-androstenedione。並重新考慮胎齡(GA)、出生體重(BW)、出生長度(BL)和17-OHP篩查結果。
對所有骨齡增加的兒童(骨齡與實際年齡之比大於1)使用可溶性Synacthen 250 mg靜脈注射ACTH刺激試驗。在基線和60分鍾後評估血清17-OHP和皮質醇水平。數據采用Maria New nomogram分析[16].
gnrh -類似物(GnRH-a)刺激試驗對具有性早熟相關體征的患者(女孩早裂或男孩睾丸容量> 4ml)進行,在夜間禁食後皮下給予0.1 mg GnRH-a(雷公雷林)。在基線和注射後4小時測定血清FSH、LH、雌二醇和睾酮水平。
血清17-OHP采用放射免疫測定法(DSL-5000活性17α-OH孕酮包覆管放射免疫測定法,Diasorin Spa Italia)測定。分析靈敏度為0.01 ng/dL,而分析內和分析間變異係數均為9.0%。
采用固相競爭性化學發光酶免疫法測定血清總睾酮、ACTH、皮質醇、Δ4-androstenedione、DHEAS、雌二醇、FSH和LH (Immulite 2000,西門子醫療診斷,Deerfield, IL, USA)。分析敏感性為:總睾酮0.05 mIU/mL (0.5 nmol/L), ACTH 1.1 pmol/L,皮質醇0.2 μg/dL, Δ4-androstenedione 1 nmol/L, DHEAS 0.3 μg/dL, FSH 0.1 mIU/mL, LH 0.05 mIU/mL,雌二醇15 pg/mL。
試驗內和試驗間變異係數分別為睾酮11.7和13.0%,ACTH 9.5和10.0%,皮質醇7.4和9.4%,Δ4-androstenedione 9.3和12%,DHEAS 4.1和6.3%,FSH 2.9和4.1%,LH 3.6%和6.7,雌二醇11.7和13%。
新生兒CAH篩查采用濾紙上幹燥的血點進行。在出生後48 - 72小時采集血液樣本。17-OHP采用免疫熒光法測定(Kit DELFIA新生兒17-羥孕酮試劑盒;Perkin Elmer, Wallac Oy,圖爾庫,芬蘭)。
這項研究是按照《赫爾辛基第二宣言》的規定進行的。在意大利,這種類型的回顧性研究不需要機構審查委員會/機構倫理委員會的批準就可以發表結果。獲得每位患者父母的書麵知情同意。
所有統計分析均使用r軟件進行,組間比較使用Student’s軟件進行t-test或Wilcoxon檢驗。數據以頻率、中位數加範圍或平均值±標準差(視情況而定)的數字表示。考慮統計學意義時p-values小於0.05。
結果
我們確定了330例恥骨早熟患者,其中269例女性(81.5%)和61例男性(18.5%)。平均診斷年齡為7.3±1.8歲。本群體的auxological數據如表所示1.其中20%為早產,GA < 37周,13.7%為低體重(< 2500克)。31%的女孩伴有恥骨裂,而隻有3%的男性患者有睾丸體積增大。172例(51.5%)表現為骨齡高齡。女性患者的骨齡比正常年齡增加1.3±1.0歲,男性患者的骨齡增加1.4±1.0歲。這172例患者進行了血液檢查,見表2.
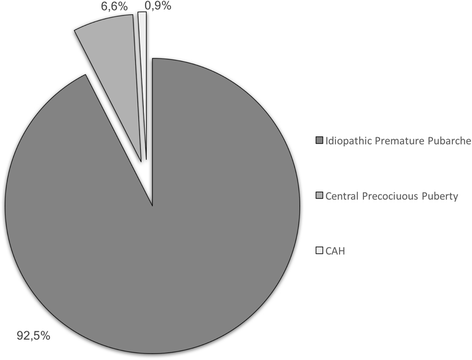
數字1代表在我們的隊列中根據ACTH測試和GnRH-a測試結果確定的恥骨病病因(數據未顯示)。此外,25名兒童(24名女性和1名男性)在ACTH測試中表現出17-OHP水平,與21-OHD的雜合條件兼容。
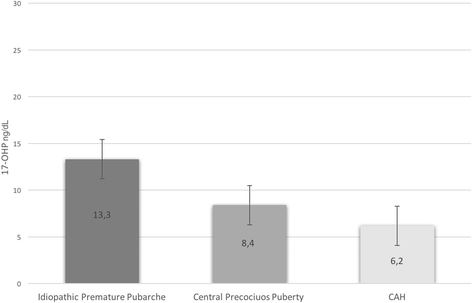
數字2表示在新生兒篩查中評估的所有早熟恥骨患者的17個OHP水平。3例遲發性CAH患者17-OHP篩查值均正常。隻有1例患者(妊娠28周早產,體重1010g)在新生兒篩查時出現17-OHP臨界值;然而,他沒有受到CAH的影響,而隻是受到特發性早熟的影響。
討論
據我們所知,這是第一個分析早產兒青春期與新生兒CAH篩查中17-OHP水平之間關係的研究。
恥骨早熟並不罕見,通常是腎上腺早期孤立性成熟的繼發性情況[17,18,19].在一些患者中,腎上腺雄激素可能在實際年齡適度增加,盡管在其陰毛階段的正常範圍內,其他患者的雄激素水平是正常的,但一些作者認為外周對雄激素的敏感性增加[17].然而,早熟的診斷是一種排除性診斷。事實上,在我們6.6%的患者中,早熟與性早熟有關,因為所有這些兒童不僅表現出早熟,而且還表現出一些初始的青春期體征。此外,必須排除遲發性CAH、其他罕見的輕度類固醇生成錯誤和雄化腎上腺或性腺腫瘤[17].
在診斷框架內,仍有爭議的患者應提交ACTH刺激試驗。一些作者建議,當骨齡與身高年齡之比超過1時,或雄激素水平升高時,或最終出現骨齡進展、囊性痤瘡或其他全身男性化檢測跡象時,患者應接受該檢查[17].當骨齡與實足年齡之比大於1時,我們決定進行ACTH測試,在此基礎上,我們確定了3名遲發性CAH患兒(1.7%)。我們的隊列中沒有人出現男性化腫瘤。
其餘兒童(占總隊列的92.5%)受到特發性早熟的影響。其中,63.5%的患者DHEAS水平升高。雖然DHEAS是一種弱雄激素,但它是合成更強雄激素的底物,且高於40-50 μg/dL的DHEAS水平與陰部的出現有關[17,19,20.].在這些患者中,過早的陰部可能源於病因不明的功能性腎上腺高雄激素血症,可能是由於腎上腺網狀帶增生所致。在另外的36.5%中,過早的陰毛的出現可能與上述外周對正常雄激素水平的敏感性增加有關。
在我們研究的早熟兒童隊列中,CAH的患病率與之前的數據相當,之前的數據估計其範圍為0 - 40% [9,20.,21,22,23,24].然而,在ACTH刺激試驗後,25名兒童(14.5%)表現出與雜合條件兼容的17-OHP水平。眾所周知,陰部早熟、多毛症和性早熟患者可能由於雜合狀態而出現21-羥化酶輕度缺乏症[25].事實上,在未受CAH影響但表現出高雄激素體征的受試者中,有很大比例的人攜帶了CYP21A2基因雜合狀態的突變[26,27,28].然而,一些作者報告突變攜帶者和野生型受試者的風險相似[29,30.],其他研究證明了高雄激素血症的臨床體征與雜合子狀況之間的關聯,特別是在攜帶V281 L突變的受試者中[31,32].已描述了該突變等位基因對野生型的顯性負作用,降低了酶活性,其後果是由於雄激素過量而導致症狀風險增加[31].雖然我們沒有對我們的25個孩子進行遺傳分析,但他們的17-OHP水平與雜合子條件相匹配,將證實雜合子條件與早熟陰部的存在之間存在關聯。這種關聯背後的真正機製仍然未知。
除1例早產外,所有陰部早產患者,包括3例非經典CAH患者,在新生兒篩查時17-OHP水平均在參考範圍內。這篇手稿中提供的數據表明,新生兒篩查時17-OHP升高並不意味著早熟風險增加。如上所述,新生兒CAH篩查不是為了檢測非經典形式的疾病,因為患有這種形式的疾病的患者的基礎血清17-OHP水平通常在正常範圍內[1,8,9,10,11].它們的識別可能需要較低的臨界值,假陽性召回率顯著增加,成本:效益比大幅上升[33].但是,是否有必要將無症狀且血清17-OHP水平僅略有升高的新生兒提交完成檢查,以排除中期CAH,在新生兒期可能不需要任何治療,而隻需隨著時間的推移進行足夠的隨訪?在之前的一篇文章中,我們得出結論,如果新生兒的血清17-OHP篩查試驗呈陽性,則無需進行進一步的調查,我們建議如果出現進一步的症狀,僅在以後進行其他確認性測試[7].其他作者建議由兒科內分泌科醫生每年進行一次隨訪,以檢查生長速度和CAH的體征[1,34,35].我們的數據允許不建議對這些新生兒進行內分泌科定期隨訪;隻有在兒童時期出現症狀時,才有必要進行進一步的內分泌檢查。
新生兒21-OHD篩查的主要缺點是假陽性率高,陽性預測值低,主要出現在早產、低BW和患病新生兒中[4,36,37,38].特別是在法國,常規21-OHD篩查在早產兒中的效率非常低,因此法國作者建議對這些新生兒中斷篩查[6].然而,為了降低假陽性率,其他篩查項目已經建立了與GA相關的17-OHP截止水平[36,39,40,41]或BW [42,43,44].我們還使用了與GA相關的截止時間[45].事實上,唯一的特發性早熟的孩子在新生兒篩查時表現出較高的17-OHP,結果不受CAH影響;然而,他出生時早產(妊娠28周),眾所周知,17-OHP水平升高在早產和低BW嬰兒中很常見[36,37,46].由於酶11-β-羥化酶的生理表達出現一定的延遲[47],在所有GA小於31周的早產兒中,篩查17-OHP水平升高而無先天性類固醇生物合成錯誤[48].在之前的一項研究中,我們假設低21-羥化酶的酶功能可能導致篩查中17-OHP水平升高,我們已經確認,這種酶的不成熟也可能存在於足月嬰兒[7].其他可能導致出生時17-OHP水平升高的因素是新生兒黃疸或新生兒疾病。事實上,由於脫水對血液濃度的影響,高膽紅素血症可能導致17-OHP值升高[49],新生兒壓力可能增加ACTH和17-OHP水平[41].
結論
總之,我們排除了在新生兒篩查中未受經典21-OHD影響的嬰兒中17-OHP升高可能是未來早熟的跡象。出生時17-OHP水平升高的主要原因仍然是腎上腺發育不成熟和/或新生兒應激。因此,在兒童時期對這些嬰兒進行嚴格的隨訪是沒有必要的。
縮寫
- 17-OHP:
-
17-hydroxyprogesterone
- 21-OHD:
-
21羥化酶缺乏
- 提單:
-
出生的長度
- BW:
-
出生體重
- 兒童和青少年衛生與發育司:
-
先天性腎上腺增生
- 遺傳算法:
-
孕齡
- GnRH-a:
-
GnRH-analogous
- SD:
-
標準差
參考文獻
ESPE/LWPES CAH聯合工作組。Lawson Wilkins兒科內分泌學會和歐洲兒科內分泌學會關於21-羥化酶缺乏症的共識聲明中國臨床內分泌雜誌,2002;
新生兒先天性腎上腺增生篩查。內分泌代謝臨床雜誌2001;30:15-30。
美國兒科學會內分泌科和遺傳學委員會。技術報告:先天性腎上腺增生。兒科。2000;106:1511-8。
Gidlöf S, Wedell A, Guthenberg C, von Döbeln U, Nordenström A.瑞典新生兒先天性腎上腺增生的全國性篩查:一項基於人群的26年縱向前瞻性研究。美國兒科雜誌,2014;168:567-74。
Grosse SD, Van Vliet G.通過新生兒先天性腎上腺增生篩查可以預防多少死亡?Horm Res. 2007; 67:284-91。
Coulm B, Coste J, Tardy V, Ecosse E, Roussey M, Morel Y, Carel JC, DHCSF研究組。1996 - 2003年在法國大陸出生的新生兒篩查21-羥化酶缺乏症引起的先天性腎上腺增生的效率兒科青少年醫學,2012;166:113-20。
Cavarzere P, Samara-Boustani D, Flechtner I, Dechaux M, Elie C, Tardy V, Morel Y, Polak M.短暫性高17-羥孕激素血症:新生兒篩查診斷為先天性腎上腺增生的臨床亞組。中華內分泌雜誌,2009;
Gönç EN, Ozön ZA, alikaiifovlu A, Engiz O, Bulum B, Kandemir N.基礎血清17-OH孕酮是預測早期腎上腺素非經典先天性腎上腺增生的可靠參數嗎?土耳其兒科雜誌,2011;53:274-80。
ArmengaudJB CML, Trivin C, Tardy V, Bréart G, Brauner R, Chalumeau M.早熟性陰部:區分遲發性先天性腎上腺增生與早發性腎上腺增生。中國臨床內分泌雜誌,2009;
gizzoni L, Cappa M, Vottero A, Ubertini G, Carta D, Di Iorgi N, Gasco V, Marchesi M, Raggi V, Ibba, Napoli F, Massimi A, Maghnie M, Loche S, Porzio O.一組意大利早熟兒童CYP21A2基因型與血清17-羥孕酮和皮質醇水平的關係中華內分泌雜誌,2011;
Livadas S, Dracopoulou M, Dastamani A, Sertedaki A, Maniati-Christidi M, Magiakou AM, Kanaka-Gantenbein C, Chrousos GP, dacouo - voutetakis C. 280例由CYP21A2基因突變引起的非經典先天性腎上腺增生的臨床、激素和分子特征。臨床內分泌雜誌2015;82:543-9。
馬修RP,拜恩DW,林頓MF,沃恩DE,法齊奧S,羅素WE。在診斷時患有早熟陰部的瘦弱兒童中代謝綜合征的證據。新陳代謝。2008;57:733-40。
Utriainen P, Jääskeläinen J, Romppanen J, Voutilainen R.兒童代謝綜合征及其早期腎上腺素的組成。中國臨床內分泌雜誌,2007;
Tanner JM, Whitehouse RH。身高、體重、身高速度、體重速度和青春期階段的臨床縱向標準。Arch Dis Child, 1976; 51:170-9。
格魯裏奇WW,派爾SI。手和手腕骨骼發育的放射學圖集。第二版。斯坦福:斯坦福大學出版社;1959.
New MI, Lorenzen F, Lerner AJ, Kohn B, Oberfield SE, Pollack MS, Dupont B, Stoner E, Levy DJ, Panq S, Levine LS。基因分型類固醇21-羥化酶缺乏症:激素參考數據。中華臨床內分泌雜誌,1983;
Ibáñez L, Dimartino-Nardi J, Potau N, Saenger P.腎上腺早衰——正常變異還是成人疾病的前兆?Endocr Rev. 2000; 21:671-96。
威廉姆斯RM,沃德CE,休斯IA。過早adrenarche。Arch Dis Child. 2012; 97:250-4。
胡曉玲,李誌強,李誌強,Jääskeläinen J,腎上腺素早衰是一種常見的疾病。《兒科雜誌》2015;83:221-31。
Ghanny BA, Malhotra S, Kumta S, Kazachkova I, Homel P, Jacobson-Dickman E, Motaghedi R.孤立性腎上腺早衰兒童是否應常規評估非經典性先天性腎上腺增生?中國兒科內分泌雜誌2016;29:351-6。
Ibáñez L, Bonnin MR, Zampolli M, Prat N, Alia PJ, Navarro MA。促腎上腺皮質激素試驗在診斷非經典21-羥化酶缺乏症中出現過早陰部的兒童的有用性。Horm Res. 1995; 44:51-6。
Korth-Schutz S, Levine LS, New MI.正常青春期前和青春期兒童以及性早熟兒童血清雄激素的研究。中華內分泌雜誌,2001;23(4):344 - 344。
Leite MV, Mendonça BB, Arnhold IJ, Estefan V, Nunes C, Nicolau W, Bloise W.非經典21-羥化酶缺乏症在女孩性早熟的鑒定。中華內分泌雜誌。1991;14:11-5。
Voutilainen R, Jääskeläinen J.腎上腺素過早:病因學,臨床表現和後果。中國生物化學雜誌,2015;
Knorr D, Bidlingmaier F, Höller W, Kuhnle U, Meiler B, Nachmann A.類固醇21-羥化酶缺乏症雜合子是否導致兒童多毛、陰部過早、性早熟和性早熟?內分泌學報(哥本哈根)。1986; 279:284-9。
Speiser PW, Dupont B, Rubinstein P, Piazza A, Kastelan A, New MI。非經典類固醇21-羥化酶缺乏症發生率高。胡姆·熱內。1985;37:650-67。
Skordis N, Shammas C, Phedonos AA, Kyriakou A, Toumba M, Neocleous V, Phylactou LA。CYP21A2基因在腎上腺早衰女孩中的遺傳缺陷。中華內分泌雜誌2015;38:535-9。
Neocleous V, Shammas C, Phedonos AP, Karaoli E, Kyriakou A, Toumba M, Phylactou LA, Skordis N. cyp21a2基因在早熟腎上腺素女孩和高雄激素血症青少年女性中的遺傳缺陷。《格魯吉亞醫學新聞》2012;210:40-7。
Knochenhauer ES, Cortet-Rudelli C, Cunnigham RD, Conway-Myers BA, Dewailly D, Azziz R. 21-羥化酶缺乏症攜帶者發生高雄激素血症的風險不增加。中華內分泌雜誌,2000;
Escobar-Morreale HF, San Millán JL,史密斯RR,桑丘J,女巫SF。多毛女性中21-羥化酶缺乏載體狀態的存在:表型-基因型相關性。《生殖科學》1999;72:629-38。
警告O,以色列S, Lavi I, Gur M, Tenenbaum-Rakover Y. CYP21突變攜帶者的高雄激素血症:基因型的作用。臨床內分泌雜誌。2006;64:645-51。
女巫SF,李PA,蘇達-哈特曼M,霍夫曼EP。21-羥化酶缺乏症表現為高雄激素血症和雜合子。生物化學與分子醫學。1997;62:151-8。
歐洲兒科內分泌學會新生兒篩查工作組。新生兒21-羥化酶缺乏性先天性腎上腺增生篩查程序。Horm Res. 2001; 55:201-5。
Merke DP, Bornstein SR.先天性腎上腺增生。《柳葉刀》雜誌。2005;365:2125-36。
白色PC, Speiser PW。21-羥化酶缺乏症導致的先天性腎上腺增生。Endocr Rev. 2000; 21:245-91。
Torresani T, Grüters A, Acherz R.根據胎齡調整17-α-羥孕酮臨界值提高新生兒先天性腎上腺增生篩查的療效。篩選。1994;3:77 - 84。
新生兒先天性腎上腺增生篩查的評價。Horm Res. 2001; 55:206-11。
貝裏J,貝茨P,伍德PJ。足月和早產新生兒血點17α-羥孕酮水平的解釋。生物化學,1986;23:546-51。
Van Der Kamp HJ, Oudshoorn CGM, Elvers BH, Van Baarle M, Otten BJ, Wit JM, Verkerk PH.新生兒先天性腎上腺增生篩查中17-α-羥孕酮的臨界值應基於胎齡而不是出生體重。中國臨床內分泌雜誌,2005;
Nordenström A, Wedell A, Hagenfeldt L, Marcus C, Larsson A.新生兒先天性腎上腺增生篩查:早產兒17-羥孕酮水平和CYP21基因型。兒科。2001;108:e68。
Gruñeiro-Papendieck L, Prieto L, Chiesa A, Bengolea S, Bossi G, Bergadá C.新生兒先天性腎上腺增生篩查方案:召回方案的調整。Horm Res. 2001; 55:271-7。
Allen DB, Hoffman GL, Fitzpatrick P, Laessing R, Maby S, Slyper A.利用體重調整標準對17-羥孕酮水平進行新生兒先天性腎上腺增生篩查的準確性提高。中華兒科雜誌,1997;130:128-33。
Olgemöller B, Roscher AA, Liebl B, Fingerhut R.先天性腎上腺增生篩查:根據年齡和出生體重調整17-羥孕酮臨界值顯著提高預測價值。中國臨床內分泌雜誌,2003;
Hayashi GY, Carvalho DF, de Miranda MC, Faure C, Vallejos C, Brito VN, Rodrigues AS, Madureira G, Mendonca BB, Bachega TA。新生兒17-羥孕酮水平根據樣本采集時的年齡和出生體重調整,可提高新生兒先天性腎上腺增生篩查的效果。臨床內分泌雜誌,2017;86:480-7。
Cavarzere P, Camilot M, Teofoli F, Tatò L.意大利東北部新生兒先天性腎上腺增生篩查:一項為期三年的項目報告。Horm Res. 2005; 63:180-6。
李敏敏,李誌強,李誌強。早產兒血清腎上腺激素濃度的研究。中國臨床內分泌雜誌,1989;29(2):349 - 349。
Hingre RV, Gross SJ, Hingre KS, Mayes DM, Richman RA。極低出生體重兒的腎上腺類固醇生成。中華內分泌雜誌,1994;
Ohkubo S, Shimozawa K, Matsumoto M, Kitagawa T.早產兒血點17- α -羥孕酮濃度分析:先天性腎上腺增生篩查的臨界值建議。中華兒科雜誌1992;34:126-33。
根啊。新生兒21-羥化酶缺陷先天性腎上腺增生篩查——CYP21分析的作用。中華臨床內分泌雜誌1999;84:1503-4。
確認
不適用。
資金
這份手稿沒有從任何公共、商業或非營利部門的資助機構獲得任何特定的資助。
數據和材料的可用性
不適用
作者信息
作者及隸屬關係
貢獻
所有作者都可以完全訪問研究中的所有數據,並對數據的完整性和數據分析的準確性負責。此外,所有作者都閱讀並批準了最終的手稿。研究構思:PC、MC。數據采集:MM、DAR、SL。數據分析與解釋:PC、RM。草稿:PC, MV。重要的手稿修改:MC, FA, RG, FT。學習協調:PC, MC, FA。
相應的作者
道德聲明
倫理批準並同意參與
這項研究是按照《赫爾辛基第二宣言》的規定進行的。在意大利,這種類型的臨床研究不需要機構審查委員會/機構倫理委員會的批準就可以發表結果。獲得每位患者父母的書麵知情同意。
發表同意書
作者已經獲得了所有患者父母的同意,發表了研究結果。
相互競爭的利益
作者聲明,不存在可被視為損害所報告的確認書公正性的競爭性利益。
出版商的注意
beplay外围下载施普林格自然對出版的地圖和機構從屬關係中的管轄權主張保持中立。
權利和權限
開放獲取本文根據創作共用屬性4.0國際許可協議(http://creativecommons.org/licenses/by/4.0/),允許在任何媒介上不受限製地使用、分發和複製,前提是您對原作者和來源給予適當的讚揚,提供到創作共用許可證的鏈接,並注明是否進行了更改。創作共用公共領域奉獻棄權書(http://creativecommons.org/publicdomain/zero/1.0/)除另有說明外,適用於本條所提供的資料。
關於本文
引用本文
卡瓦澤爾(P.),毛羅(M.),文生齊(M.)et al。陰部早熟兒童:改變的新生兒17-Ohp篩查試驗是一個預測因素嗎?兒科J醫院44, 10(2018)。https://doi.org/10.1186/s13052-018-0444-6
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-018-0444-6
關鍵字
- 過早pubarche
- 17-Ohp
- 新生兒篩查
- 先天性腎上腺增生