摘要
背景
當同時診斷生長激素缺乏時,應考慮用重組人生長激素治療粘多糖(MPS)影響的患者。考慮到與疾病相關的骨骼畸形的自然進展和文獻報道的治療患者的缺乏,重組人類生長激素在這個選定隊列中的短期和長期影響仍存在爭議。本病例係列提供了診斷為生長激素缺乏症的MPS患者對重組生長激素反應的詳細信息。
例演示
回顧性分析4例MPS女性患者(目前年齡:11.7-14.3歲)因生長激素缺乏而接受重組人生長激素治療後的生長模式。2例診斷為MPS IH的患者在早期進行了造血幹細胞移植;其餘2例患者受MPS IV和VI影響,采用酶替代治療。
4/4患者在確診生長激素缺乏症前表現為進行性生長減速。這一趨勢最初被一個顯著的增加高度速度後開始重組生長激素逆轉。我們記錄到,在治療6個月和12個月後,身高速度z評分平均分別為+ 4.23±2.9和+ 4.55±0.96。在最初的12-24個月後,所有患者的生長都出現了減速。而在一名攜帶MPS IH重組人生長激素的女孩中,由於缺乏臨床療效而停用,3/4的患者以穩定的速度生長,跟蹤被引用的初始身高速度增加後的身高百分位。
此外,通過骨密度測定法評估的礦物骨密度顯示,在開始治療前和後進行測試的兩名患者顯著增加。
結論
重組人生長激素似乎有效地逆轉了MPS患者所經曆的生長減速,被診斷為生長激素缺乏,至少在治療的前12-24個月。
背景
粘多糖(MPS)是一種異質性的遺傳性溶酶體儲存障礙,其原因是參與黏多糖(或糖胺聚糖(GAG))降解過程的溶酶體酶活性存在缺陷。隨後不同GAG的積累導致臨床進展性疾病,並伴有多係統並發症。
大多數MPS患者都會經曆不同程度的生長停滯和身材矮小[1].MPS中身材矮小的發病機製尚不完全清楚,盡管軟骨和骨骼的漸進性積累被認為是這些患者骨骼異常的“原發誘因”。Simonaro和他的同事報道說,GAG的儲存會引發複雜的二級和三級效應,導致炎症、軟骨細胞凋亡和滑膜增生,導致組織不良和代謝異常的結締組織基質[2].這種細胞功能的破壞被認為是彌漫性骨骼畸形(如脊柱後凸、脊柱側彎、膝外翻)及減少MPS的生長潛力。代謝和內分泌(生長激素缺乏、青春期早熟、甲狀腺功能減退)異常也在許多病例中被報道導致生長減慢[3.,4,5].
經酶替代療法(ERT)加造血幹細胞移植(HSCT)治療的MPS患者,如果受MPS IH (Hurler綜合征)影響,或僅受ERT時受MPS IH /S (Hurler/Scheie綜合征)、MPS IS (Scheie綜合征)、MPS II (Hunter綜合征)、IV (Morquio綜合征)和VI (Maroteaux-Lamy綜合征)影響,其腹部、呼吸和心血管特征均有顯著改善[6,7];然而,HSCT和ERT對肌肉骨骼係統和生長的影響往往不令人滿意[6,8].Harmatz和他的同事曾報道過,接受ERT的MPS VI患者的身高標準差評分(SDS)早期輕度增加[9];Jones和他的同事描述了被診斷為MPS II的受試者對ERT的類似反應[10].然而,報道的結果是年齡依賴的,ERT對身高增加的整體影響是有限的。
鑒於所描述的輻射對最終身材的有害影響,對移植後生長的評估可能會導致在移植前全身照射(TBI)是調節計劃的一部分的患者得出誤導的結論[11].
隻有少數手稿報道了在含有粘液多糖的GH缺乏患者中開始重組人生長激素(rhGH)後的生長模式和最終副作用:Polgreen和同事提供了大約6 MPS IH患兒接受rhGH治療的數據,其中隻有2人GH缺乏,而4人在GH刺激試驗中正常反應(GH峰值> 10微克/L):治療組和未治療組之間的身高速度沒有顯著差異,盡管與非gh缺乏組相比,gh缺乏組對治療的反應更好[12].Rogers和同事描述了一個被診斷為MPS I H/S的患者,在開始使用重組生長激素後,她的線性生長明顯改善[13].有報道1例生長激素缺乏(GHD)及MPS II患者[3.],而目前還沒有關於ghr缺乏的MPS III、IV、VI和VII受試者的公開數據。
為了描述MPS患者因GHD而接受rhGH治療的生長模式和矯形結果,我們在此報告了4名潛在診斷為MPS IH(2名受試者)、MPS IV和MPS VI的gh缺乏受試者。
患者和方法
在蒙紮代謝中心隨訪的64例MPS患者中,4例女性MPS患者(2例MPS IH, 1例MPS IV, 1例MPS VI;目前年齡:11.7-14.3歲),發現gh缺乏,因此開始接受rhGH治療。
臨床資料、放射資料和營養不良資料均回顧性收集於患者的臨床報告和紙質生長圖表。由一名經驗豐富的兒科內分泌學家(NM)評估站立高度、體重和坦納階段。站立高度用壁掛式測量儀(不穿鞋)測量到最接近0.1 cm;體重測量到最接近0.1 kg。
使用Lily’s Growth4®軟件根據CDC 2002年生長圖計算生長百分位和身高標準差(SDS, z-scores)。對於MPS IV和MPS VI患者,我們還在Morquio和Maroteaux-Lamy患者的疾病特異性生長曲線上繪製了患者的身高[14,15].對於MPS VI患者,采用LMS方法根據疾病特異性生長圖計算身高SDS [16].
“大酒店”狀態通過精氨酸和地塞米鬆或胰島素耐量試驗(ITT)進行評估;GHD定義為在兩個不同的天內進行的兩個連續試驗中,GHD反應不足(2010年之前GHD峰值< 10,2010年之後GHD峰值< 8微克/升)。使用DiaSorin Liaison®XL檢測GH水平。
精氨酸靜脈滴注30分鍾(劑量:0.5 g/kg,最大30 g),並在以下時間點提取GH和血糖血樣:−15分鍾,時間0,+ 30分鍾,+ 45分鍾,+ 60分鍾,+ 75分鍾,+ 90分鍾,+ 105分鍾和+ 120分鍾。
靜脈給予地塞米鬆2 mg/m2;分別於+ 60′、+ 90′、+ 120′、+ 135′、+ 150′、+ 165′、+ 180′、+ 195′、+ 210′、+ 225′、+ 240′采集GH評價血液樣本。
最後,在ITT期間,根據基線血糖水平(0.05 ~ 0.1 IU/kg),靜脈注射常規胰島素(可變劑量)。當出現以下至少一種情況時,胰島素誘導的低血糖刺激被認為是足夠的:血糖水平下降到45 mg/dL或更少;血糖水平較基礎值降低至少50%;孩子出現了症狀。在以下時間點提取GH和血糖水平的血液樣本:−20分鍾,時間0,+ 20分鍾,+ 30分鍾,+ 45分鍾,+ 60分鍾,+ 90分鍾和+ 120分鍾。
根據兒科內分泌學會提供的適應症[17],由於我們的患者年齡小於10歲,所以我們不進行刺激性生長激素測試前的性類固醇啟動。
考慮到正常值隨性別、年齡和實驗室檢測結果的差異,我們根據每個試劑盒的年齡和性別調整的參考範圍(下截止點:−2個SDS,上截止點:+ 2個SDS)記錄IGF-1水平作為標準差評分(IGF-1 SDS)。
rhGH的劑量與診斷為GHD的非mps受試者相同,即0.025-0.035 mg/kg/die或5-7 mg/m2/周。
患者的平均治療時間為3.3±1.9年(範圍為3.0 - 6.2)。
每6個月(±1個月)對接受rhGH治療的患者進行係統的臨床和體征評估。高度速度的估計時間間隔不少於6個月;高度速度SDS根據WHO 2006年圖表計算。
在發表病例係列和伴隨圖像時,獲得患者監護人的知情同意。
案例係列
赫爾綜合征(MPS 1H)
2例MPS 1H患者被診斷為GHD並在本中心接受rhGH治療。他們都在出生後的最初幾個月接受了ERT治療,隨後進行了早期造血幹細胞移植。這兩名患者在造血幹細胞移植前均接受了布蘇芬/環磷酰胺為基礎的清髓治療方案。
患者1在15個月大時開始接受ERT,在20個月大時接受HSCT。由於植入物過早丟失,在2.8歲時成功進行了第二次HCST,在隨後11年的隨訪中,足夠的循環酶水平證實了植入物的穩定持久性。
在6.7歲時,臨床複查時生長逐漸減速(身高速度:1.8 cm/年,−5.14 SDS), IGF-1水平低於−2 SDS,骨齡明顯延遲(4.5歲,而實際年齡為6.7歲),促使臨床醫生進行了arg和地塞米鬆刺激試驗,確診為GH缺乏(GH峰值分別達到7.9和4.4微克/升)。
MRI顯示下丘腦-垂體區正常。
因此,她開始接受標準劑量的rhGH (0.025 mg/kg/die),隨後在隨後的生化隨訪中,IGF-1水平歸一化,IGF-1 SDS持續在+ 1.5 - + 1.9 SDS之間。
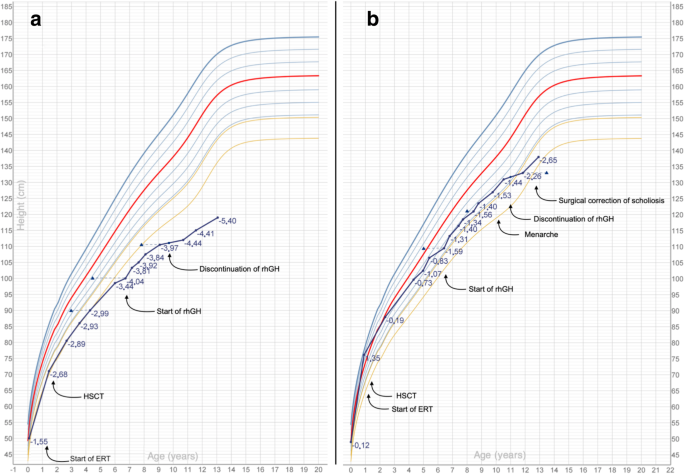
數字1a為患者開始rhGH前後的生長曲線圖。在6個月(4.3 cm/年,−2.11 SDS)和12個月(5.2 cm/年,−0.60 SDS)隨訪時記錄的高度速度顯著增加,導致高度SDS輕度改善(治療12個月後從−3.57到−3.42 SDS)。雖然在治療的前1.5年,上述身高SDS的下降被開始服用rhGH中斷,但隨後注意到身高SDS的進一步進行性下降,並導致臨床醫生在9.6歲時停止重組GH治療,考慮到整體的遲發反應較差(治療總時長:2.9年)。患者是青春期前(Tanner的階段:B1P1A1),在開始治療之前,青春期發展的第一個早期跡象是在停止rhGH後被注意到的。
從矯形學的角度來看,早期發現的骨骼異常在整個兒童期逐漸惡化。
開始rhGH前2年發現雙側髖股半脫位(右>左)。在開始治療後2年和停止治療前1年,發現腿長差異約1厘米。在最後的矯形隨訪中(rhGH停用3年後),差異增加到2厘米。
同時兩國膝外翻逐漸惡化,但大部分進展發生在停止rhGH後:治療前的- 8°脛股角在治療結束6個月後下降到- 10°,最後骨科隨訪時達到- 12/ - 15°,大約3年後。
該患者自4歲起就已出現多椎體畸形和T12-L1椎體滑脫。
放射學隨訪顯示,大約在rhGH停用1.5年後矢狀椎體排列進一步惡化。6個月後(停用rhGH後2年),患者開始抱怨偶發性腰痛和下肢功能減退;體格檢查時描述反射不足和後凸的進展。臨床錐體征的出現提高了手術治療的嚴格指征,在12.1歲。
患者2在13個月時開始ERT, 3個月後進行HSCT。患者在6.4歲時被診斷為生長激素缺乏(精氨酸試驗生長激素峰值:6.0微克/升;胰島素耐量試驗時生長激素峰值:7.8微克/升)。診斷為生長激素缺乏時,患者的骨年齡略微延遲(5.0歲,而實際年齡為6.4歲)。MRI未見下丘腦-垂體區異常。
rhGH開始後,高度速度顯著增加:從0時的2.96 cm/年(−3.44 SDS)到6個月後的9.97 cm/年(+ 4.56 SDS),以及治療第一年結束時的6.99 cm/年(+ 1.21 SDS)。患者在5 - 6年期間經曆的身高SDS的最初下降被重組GH的開始打斷,患者的生長持續跟蹤第10百分位,直到10.1歲,她達到初潮。當她11.0歲時停止使用rhGH治療,因為年身高速度下降到2厘米/年以下。在治療期間,IGF-1水平從基線水平−1.7 SDS上升到+ 1.3-1.7 SDS。
數字1B顯示該患者的生長模式。在rhGH停止後,身高陡增是她在生長結束時接受脊柱手術幹預的結果。
從矯形學角度來看,雙頸椎後彎和腰椎側彎在rhGH治療前就已被發現。在停止rhGH期間和之後進行了年度隨訪,沒有脊柱畸形惡化的報告。如前所述,患者在生長結束時成功地接受了選擇性脊柱後凸性脊柱側彎手術矯正。
在出生後的第二年,髖關節x光片顯示最初的髖股半脫位。放射學隨訪顯示,在開始rhGH之前,這些畸形逐漸惡化,右股骨頭受損傷更明顯,隨後腿長差異增加。生長結束時,右股骨頭半脫位在放射學上更為明顯,但從未發展為明顯脫位。
莫爾奎奧綜合征(MPS IV)
本中心發現1例Morquio綜合征患者存在gh缺乏(患者3)。
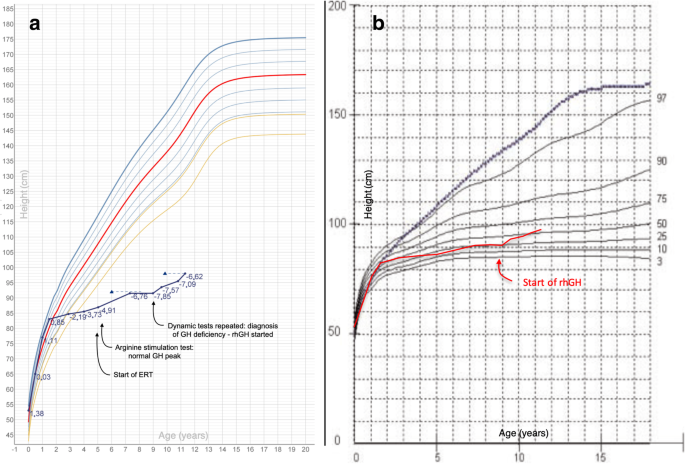
如圖所示。2在出生後的第一年,患者在早期滿意的生長後,經曆了顯著的身高速度下降。她在5.3歲時接受了精氨酸刺激試驗,這提供了一個正常的高峰。在生長完全停止7.3 - 8.9年之後,患者再次接受檢查,證實生長激素缺乏(精氨酸試驗:生長激素峰值5.7微克/升;地塞米鬆試驗:GH峰值6.1微克/升)。放射學發現骨齡明顯延遲(6歲,而實際年齡8.3歲)與GH缺乏的診斷一致。
圖示:CDC繪製的患者3的生長模式(一個)和特定疾病生長圖表(b,源自參考文獻[14])。在一個,藍點代表年齡的身高;每次測量的高度SDS用藍色表示;藍色三角形代表骨齡的高度。在b虛線表示未受影響的女孩身高的第50厘
rhGH啟動前的基線IGF-1 SDS為−2.1 SDS。MRI顯示蝶鞍和蝶骨的畸形外觀,與MPS形態一致,腺垂體和神經垂體的解剖和體積均正常。
開始使用rhGH(初始劑量:0.027 mg/kg/die)後,24個月後的最後一次臨床隨訪時,身高速度顯著增加,從0.16 cm/年(−6.12 SDS)增加到3.33 cm/年(−1.33 SDS)。這些形態學發現與IGF-1 SDS在治療期間的正常化(+ 1.0至+ 1.5 SDS)相一致。
因此,通過激素替代治療,身高SDS在4.1歲至8.9歲之間的進行性下降得以恢複。2a和b)。
從骨科的角度來看,患者在接受rhGH治療24個月後沒有出現任何並發症。膝外翻在患者開始激素治療前進行了手術矯正,在隨後的放射隨訪中沒有描述任何變化;髖valga在開始rhGH之前被診斷,之後沒有進一步惡化描述。
此外,在啟動rhGH後1年和2年重複雙能x線骨密度測定(DXA)掃描顯示骨密度的漸進式改善:啟動rhGH前1個月觀察到的總體骨密度z評分從−4.9提高到−3.7(1.6年後)和−2.3(2.4年後)。
馬羅托-拉米綜合征(MPS VI)
一名女性患者由於在我們中心發現生長激素缺乏而開始服用rhGH(患者4)。該兒童在出生後的頭幾年有規律地生長(追蹤普通人群的第50百分位- CDC生長圖表)。6歲以後,她的身高SDS開始出現進行性下降。8.8歲時,她接受了GH刺激試驗,確診為GH缺乏(精氨酸試驗:GH峰值3.7微克/升,地塞米鬆試驗:GH峰值7.4微克/升)。手和手腕x光,在診斷生長激素不足,顯示骨年齡為7.8歲。MRI未發現鞍區或鞍旁異常。
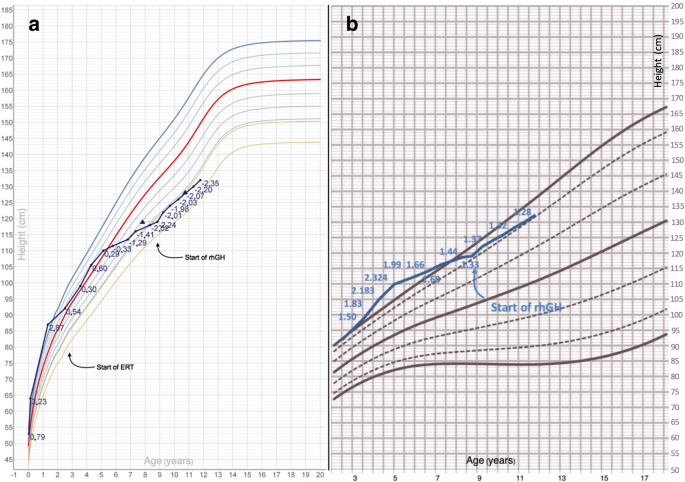
患者在8.8歲時開始接受rhGH治療。治療開始後,高度速度顯著增加(6個月後從−4.32 SDS增加到−0.95,治療第一年結束時增加到+ 0.95)。這種反應逆轉了先前的身高SDS逐漸下降的趨勢,因此隨後出現了規律的增長(在疾病特異性圖表中,身高在8.8 - 11.75年之間穩定在+ 1.3 SDS左右,最後的臨床隨訪)。3.在啟動rhGH之前(+ 1.1 SDS)和之後(+ 1.4 ~ 1.9 SDS) IGF-1 SDS值均在正常範圍內。
圖示:CDC繪製的4號病人的生長模式(一個)和特定疾病生長圖表(b,源自參考文獻[15])。在一個,藍點代表年齡的身高;每次測量的高度SDS用藍色表示;藍色三角形代表骨齡的高度
從矯形學的角度來看,在出生後的頭幾年診斷為背腰椎側彎的患者采用保守的背部支架治療。此外,膝外翻在開始生長激素替代治療前確診,接受半骺融合手術治療,短期和長期預後良好;整體矯形圖像顯示,在3.8年的rhGH治療後沒有進展的跡象。
最後,在開始rhGH前和2.1年後進行的DXA掃描顯示骨密度顯著增加(總體骨密度z-評分從−1.4到−0.5)。
討論
在本病例係列中,我們提供了4例MPS患者因證實有GHD而接受rhGH治療的詳細的人體測量和骨科數據。
一些作者已經分析了rhGH在受粘多糖影響的患者中的作用,但大多數數據來自大多數非生長激素缺乏患者的隊列[3.,12,13,18].與大多數國家一樣,重組生長激素的治療僅被許可用於已證實生長激素分泌不足的患者,由於非生長激素缺乏和生長激素缺乏患者對rhGH的反應預計會有所不同,我們重點關注後一類患者。
臨床標準所有患者生長減速或生長完全停止引起生長激素的懷疑,導致臨床醫生進行生長激素動態試驗。
在開始rhGH治療後的6個月和12個月,所有患者的身高速度SDS顯著增加(平均Δ身高速度SDS: 6個月時+ 4.23±2.9,12個月時+ 4.55±0.96),逆轉了之前的身高SDS進行性下降的趨勢。與大多數接受rhGH治療的健康患者一樣,2年後,身高-速度SDS開始出現初始下降(Δ身高-速度SDS: + 3.2±1.12)。在一名被診斷為MPS IH並接受HSCT治療的患者中,對rhGH的最初反應隨後是身高速度的進行性下降,因此在2.9年的治療後停止治療。
我們的經驗和文獻支持至少在治療的前2年,rhGH在增加被證實生長激素缺乏的MPS患者的身高速度和逆轉身高SDS進行性下降方麵的可能療效。
在一組23名Hurler和Hunter病患者的隊列中,Polgreen和他的同事們發現,接受治療和未接受治療的受試者在身高速度上存在非統計意義上的顯著差異[12].相反,我們的兩位MPS IH患者在治療的第一年表現出顯著的身高速度增加(分別從1.8到5.32 cm/年和從2.96到6.99 cm/年)。這種明顯的差異可能是由於引用的論文中的研究人群大多包括了生長激素分泌正常的患者,因為隻有4名兒童被證實存在生長激素缺乏。
納入的MPS IH患者均在布舒芬/環磷酰胺條件作用後接受了造血幹細胞移植。雖然TBI對生長的有害作用已被廣泛描述,但曆史上一直認為,以布舒泮/環磷酰胺為基礎的方案不會影響HSCT後的最終身高[19,20.].就在最近,Bakker和他的同事提出的數據表明,在接受基於布舒芬的方案治療的患者中,生長激素分泌可能受損的程度是一致的,但關於rhGH在該隊列患者中的影響的數據很少[21].因此,引用的條件調節方案對患者1和2的生長減速以及患者1中記錄的對rhGH的不良反應的作用既不能確認也不能排除。
已知MPS I患者的生長早期下降,在30個月左右下降到三厘位[22].
Montano和他的同事描述了312例Morquio病兒童的進行性生長衰竭[14].成年男性的平均身高為122.5±22.5 cm,女性為116.5±20.5 cm。在MPS IV患者中,盡管早期兒童的身高正常,但在平均4歲時,身高下降到−2 SDS以下,明顯早於MPS IH和MPS II患者[12].
已發表的報告表明,MPS VI嬰兒和學步兒童在出生後的第一年生長速度正常到加速,然後在第二年生長速度下降[23].根據美國疾病控製與預防中心(CDC)的生長圖表,正常人群三歲後的身高中位數低於年齡調整後的同齡人的身高第5百分位[15].
文獻中沒有關於MPS IV或MPS VI的gh缺乏患者的數據。Polgreen和同事描述了一名Morquio病患者和一名Maroteaux-Lamy綜合征患者使用rhGH的人體測量數據,但是,他們對GH刺激試驗的反應是正常的[3.].據我們所知,我們在這裏描述了第一例因證實的GHD而接受rhGH治療的MPS IV和MPS VI患者;我們的數據表明,身高SDS和身高速度SDS均有早期反應。
考慮到廣泛描述的GAG在骨骼和生長板中的病理積累的有害影響,rhGH在提高高度速度方麵的早期有效性並不是一個明顯的結果。
在我們機構隨訪的MPS患者中,生長激素缺乏的患病率顯著高於普通兒科人群(1:4000-1:8000兒童)[24,25].我們推測這可能與HSCT對GH分泌和垂體中GAG沉積的不利影響有關[21].
生長激素缺乏的診斷需要結合生長發育學(身高SDS、身高速度SDS)、臨床和生化(動態試驗後獲得的生長激素峰值)數據。由於生長減速至少可以部分歸因於粘多糖病本身,有人可能會認為我們的患者(被診斷為輕度GHD, MRI的放射學檢查結果正常)不能明確標記為GHD缺乏。實際上,所有的患者都接受了生長激素刺激試驗,因為他們的生長完全停止或嚴重的生長減速,即使與MPS人群相比,這也是意料之外的。因此,我們認為生長激素缺乏的診斷既符合生長學標準,又符合生化標準。
在診斷生長激素缺乏時,與實際年齡相比,所有入選兒童的骨年齡顯著延遲,這與生長激素缺乏患者的預期結果一致。隨後的放射學隨訪,見圖。1,2而且3.研究顯示,實足年齡和骨齡之間的差距逐漸縮小,在青春期前的兒童中也是如此。骨成熟被廣泛描述為rhGH對其他健康兒童診斷為GHD的影響,但眾所周知,它不會影響一般兒科人群的生長潛力[26],至少在青春期前gh缺乏的患者中,rhGH劑量不大於0.035 mg/kg / d。在MPS患者中,rhGH對最終身高的影響以及rhGH誘導的骨成熟的作用尚未得到專門的評估。需要進一步分析;然而,據報道MPS患者的腕骨發育不良[27]可能會導致對這些個體骨齡的評估產生誤導。
對於多發骨骼異常患者使用rhGH的擔憂已引起關注,因為據報道,高度速度的增加是該組患者發生大股骨骺滑移(SCFE)以及脊柱側彎和後凸進展的主要危險因素[18].
關於rhGH對非綜合征患者脊柱側彎的潛在有害影響的報道存在矛盾,大多數結果支持其安全性[28,29].de Lind van Wijngaarden和他的同事在隨機試驗中發現,在與脊柱側彎患病率較高相關的基礎疾病患者中,接受rhGH治療的Prader-Willi患者與未接受治療的患者相比,脊柱彎曲沒有顯著惡化[30.];然而,MPS患者骨骼異常的複雜性和嚴重程度可能不允許在這些患者中係統地推廣同樣令人放心的結論。
從骨科角度來看,考慮到該病的自然史,以及可能的骨科並發症的進展僅部分與rhGH的治療相一致,因此無法得出關於該患者GH對骨骼影響的明確結論。
在最後的臨床隨訪中,沒有一例患者出現明顯的SCFE。
此外,所有在替代治療期間或之後顯示進展的骨科異常在開始rhGH之前就已經被診斷。1例患者在開始使用rhGH後,經曆了放射學和臨床上的漸進性後凸惡化,這導致了矯形矯正手術。
在開始治療前後,四分之二的患者可以進行DXA掃描,他們的骨密度顯示出顯著的改善:這些結果與生長激素對骨礦化的積極作用一致,文獻中已經描述過[31].
我們意識到我們分析的潛在局限性:其回顧性性質和小樣本量可能會影響得出結論的重要性。特別是,rhGH的潛在有害影響不能在小型病例係列中進行評估。然而,當我們在一組被診斷為同時患有兩種罕見疾病(即GHD和MPS)的患者中分析rhGH的影響時,我們相信所提供的信息可能會在科學界引起有趣的討論。
結論
總之,我們的病例係列強調,在gh缺乏的MPS患者開始rhGH後,至少12-24個月的身高速度顯著增加。不管MPS的具體類型是什麼,隻要GH缺乏被證明是導致身高SDS隨著時間的推移而無法解釋的下降的原因,rhGH是一種有用的工具,可以逆轉身高的遞進下降。在我們的患者中,既不能證明也不能排除矯形畸形的進展與rhGH治療之間的相關性,需要進一步的數據來評估任何最終相關性;然而,rhGH似乎對MPS患者的骨礦化也有積極作用。
考慮到已證實的rhGH的早期益處,我們建議診斷為GHD的MPS患者開始使用rhGH。然而,需要更大規模的研究來評估rhGH對MPS患者最終身高的影響。
數據和材料的可用性
在這項研究中產生或分析的所有數據都包含在發表的文章中。
縮寫
- 用:
-
雙能x線吸收儀
- 導:
-
酶替代療法
- 嘔吐:
-
粘多糖
- “大酒店”:
-
生長激素
- GHD:
-
生長激素缺乏症
- HSCT:
-
造血幹細胞移植
- ITT公司:
-
胰島素耐量試驗
- 議員:
-
黏多醣症
- rhGH:
-
重組人生長激素
- SCFE:
-
大股骨骺滑動
- SDS:
-
標準偏差的分數
- 創傷性腦損傷:
-
全身輻照
參考文獻
張誌強,張誌強,張誌強,等。粘多糖對植物生長的影響。《科學通報》。2018;124:1-10。
Simonaro CM, D'Angelo M, He X, Eliyahu E, Shtraizent N, Haskins ME, Schuchman EH。糖胺聚糖介導的骨關節疾病的機製:對粘多糖和其他結締組織疾病的影響。潘文華。2008;172:112-22。
Polgreen LE, Miller BS。粘多糖的生長模式和生長激素的使用。兒科康複醫學雜誌2010;3:25-38。
Concolino D, Muzzi G, Pisaturo L, Piccirillo A, Di Natale P, Strisciuglio P.兩例新病例在Sanfilippo IIIA性早熟中的診斷和隨訪。中華醫學雜誌。2008;51:466 - 471。
Nour MA, Luca P, Stephure D, Wei XC, Khan a .兩例hunter綜合征患者的前側垂體功能減退與治療反應的比較。兒科病例代表。2016;2016:1 - 5。
Aldenhoven M, Jones SA, Bonney D, Borrill RE, Coussons M, Mercer J, Bierings MB, Versluys B, van Hasselt PM, Wijburg FA, van der Ploeg AT, Wynn RF, Boelens JJ。造血細胞移植治療粘多糖病安全有效:國際指南實施後的結果。骨髓移植。2015;21:1106-9。
李誌強,李誌強。酶替代療法:療效和局限性。中國兒科雜誌。2018;44:120。
Gardner CJ, Robinson N, Meadows T, Wynn R, Mercer J, Church HJ, Tylee K, Wraith JE, Clayton PE。英國人群中投擲者綜合征(MPS1H)患者的生長、最終身高和內分泌後遺症。J Inherit Metab Dis. 2011; 34:489-97。
Harmatz P, Hendriksz CJ, Lampe C, McGill JJ, Parini R, Leão-Teles E, Valayannopoulos V, Cole TJ, Matousek R, Graham S, Guffon N, Quartel A.乳糖酶替代療法對粘多糖病VI (Maroteaux-Lamy綜合征)患者生長的影響。《科學》2017;122:107-12。
Jones A, Parini R, Harmatz P, giuliani R, Fang J, Mendelsohn NJ。硬硫酶對獵人綜合征患者生長的影響:來自獵人結局調查(HOS)的數據。《科學》2013;109:41-8。
Polgreen LE, Tolar J, Plog M, Himes JH, Orchard PJ, Whitley CB, Miller BS, Petryk A.造血幹細胞移植後hurler綜合征患者的生長和內分泌功能。骨髓移植。2008;41:1005-11。
Polgreen LE, Thomas W, Orchard PJ, Whitley CB, Miller BS。重組人生長激素對1-2歲投擲者或獵人綜合征兒童身高、骨密度和體組成變化的影響張誌強。2013;11:61 - 68。
生長激素治療hurler-Scheie綜合征患者。中華兒科雜誌。2014;27:957-60。
莫爾奎奧A病患者的生長曲線圖。中國醫學雜誌。2008;10:1286-95。
Quartel A, Hendriksz CJ, Parini R, Graham S, Lin P, Harmatz P.粘多糖病VI (Maroteaux-Lamy綜合征)個體生長圖表。JIMD眾議員18:1。2014;
科爾TJ。利用LMS方法測量了NCHS和荷蘭國家身高標準中的偏度。Ann Hum Biol. 1989; 16:407-19。
Grimberg A, DiVall SA, Polychronakos C, Allen DB, Cohen LE, Quintos JB, Rossi WC, Feudtner C, Murad MH.兒童和青少年生長激素和胰島素樣生長因子- 1治療指南:生長激素缺乏症、特發性矮小和原發性胰島素樣生長因子- 1缺乏症。中國兒科雜誌。2016;86:361-97。
劉誌強,劉誌強,劉誌強,等。造血細胞移植後兒童hurler綜合征的短期生長激素治療。骨髓移植。2009;44:279-85。
Cohen A, Rovelli A, Bakker B, Uderzo C, van Lint M, Esperou H, Gaiero A, Leiper A, Dopfer R, Cahn YJ, Merlo F, Kolb HJ, Socié G.兒童時期接受骨髓移植治療血血病患者的最終身高:晚期影響工作組- ebmt的研究。血。1999;93:4109-15。
Giorgiani G, Bozzola M, Locatelli F, Picco P, Zecca M, Cisternino M, Dallorso S, Bonetti F, Dini G, Borrone C. busulfan和全身照射對青春期前接受骨髓移植兒童生長的作用及重組人生長激素治療的結果。血。1995;86:825-31。
巴克B,奧斯迪克W,布雷斯特斯D,瓦倫坎普MJE,沃森JM,威特JM。嬰兒期和兒童期基於布舒番的造血幹細胞移植調節後的生長和內分泌功能紊亂。骨髓移植。2004;33:1049-56。
Różdżyńska-Świątkowska A, Jurecka A, Cieślik J, Tylki-Szymańska A. I和II型粘多糖病兒童的生長模式。世界兒科雜誌。2015;11:226-31。
Heron D, Baumann C, Benichou JJ, Harpey JP, Le Merrer M. 2例生長加速和骨成熟晚期患者的Maroteaux-Lamy綜合征的早期診斷。中華兒科雜誌。2004;63:323 - 326。
鮑小蘭,史雲峰,杜永昌,劉銳,鄧勁雲,高三明。北京市兒童生長激素缺乏症患病率調查。中華醫學雜誌1992;105:401-5。
生長激素缺乏是一個可行的診斷嗎?中國臨床內分泌雜誌1997;82:349 - 351。
薑MJ,金安英,沈ys。特發性生長激素缺乏和特發性身材矮小患者接受生長激素治療3年期間影響骨齡成熟的因素:LG生長研究數據分析醫學(巴爾的摩)。2019; 98: e14962。
粘多糖的骨科方麵。風濕病學。2011;50:26-33。
Day GA, McPhee IB, J批次,Tomlinson FH。澳大利亞生長激素治療方案中矮小兒童的生長速度和脊柱側彎的患病率和進展。脊柱側凸。2007;2:1748 - 61。
Quigley CA, Gill AM, Crowe BJ, Robling K, Chipman JJ, Rose SR, Ross JL, Cassorla FG, Wolka AM, Wit JM, Rekers-Mombarg LTM, Cutler GB。生長激素治療兒童特發性矮小的安全性。中華內分泌雜誌。2005;90:5188-96。
de Lind van Wijngaarden RFA, de Klerk LWL, Festen DAM, Duivenvoorden HJ, Otten BJ, Hokken-Koelega ACS。生長激素治療Prader-Willi綜合征兒童脊柱側彎療效的隨機對照試驗。中華內分泌雜誌。2009;94:1274-80。
Capozzi A, Casa SD, Altieri B, Pontecorvi A.生長激素缺乏(GHD)青少年骨密度低。中國骨科雜誌。2013;10:203-5。
確認
我們非常感謝蒙紮聖傑拉爾多醫院兒科主任Andrea Biondi教授和兒科護士們。特別感謝罕見代謝病股秘書Vera Marchetti女士的持續幫助,並感謝米蘭“Pierfranco e Luisa Mariani”基金會對我們的臨床和研究活動的慷慨資助。
資金
這項研究沒有從任何公共、商業或非營利部門的資助機構獲得任何特定的資助。
作者信息
作者和聯係
貢獻
RP和NM構思了展示案例係列的想法。AC和SM負責數據的收集和分析。AC和RP起草了初稿。NM、AR和SG對手稿進行了修改,並積極地增加了具體的章節,對重要的知識內容進行了嚴格的修改。所有作者均同意並最終認可所提交的稿件版本。
相應的作者
道德聲明
倫理認可和同意參與
不適用。這項研究不需要EC的批準,因為所有的試驗都被認為是臨床管理患者所必需的。
同意出版
本病例報告的發表和本病例係列圖像的使用均獲得患者父母/監護人的書麵知情同意。
相互競爭的利益
作者聲明他們沒有競爭利益。
額外的信息
出版商的注意
beplay外围下载施普林格《自然》對出版的地圖和機構附屬關係中的管轄權要求保持中立。
權利和權限
開放獲取本文根據知識共享署名4.0國際許可協議(http://creativecommons.org/licenses/by/4.0/),它允許不受限製地在任何媒體上使用、分發和複製,前提是您要適當地注明原作者和來源,提供創作共用許可的鏈接,並說明是否進行了更改。知識共享公共領域轉讓豁免書(http://creativecommons.org/publicdomain/zero/1.0/)適用於本文提供的數據,除非另有說明。
關於這篇文章
引用這篇文章
卡托尼,A.,莫塔,S.,馬賽拉,N.。et al。重組人生長激素在粘多糖和生長激素缺乏患者中的使用:一個病例係列。斜體字J Pediatr45歲的93(2019)。https://doi.org/10.1186/s13052-019-0691-1
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-019-0691-1
關鍵字
- 黏多醣症
- 垂體性侏儒症
- 人類生長激素
- 未能茁壯成長