摘要
背景
22q11.2缺失綜合征是最常見的基因組疾病之一,其特征是麵部畸形、先天性心髒缺陷、齶咽功能不全/齶裂、胸腺發育不全/發育不全、免疫缺陷、甲狀旁腺發育不全、發育遲緩、學習障礙、精神障礙、腎髒、眼部和骨骼畸形、聽力損失和喉部異常。染色體微陣列(CMA)雜交是最常用的診斷測試之一,但作為全基因組分析,它可以指出相關的偶然拷貝數變化。
案例展示
我們報告的情況下,一個兩歲的男孩來我們的注意輕度精神運動遲緩,生長不良,和輕微的麵部異常。考慮到22q11.2缺失綜合征的診斷,我們進行了CMA,不僅確認了我們的診斷,而且指出了額外的新生5q21.3q22.2微缺失,包括APC基因。由於基因檢測的結果,我們將患者納入了一個量身定製的監測方案,以實現肝母細胞瘤的早期檢測。兒童接受手術和化療,癌症完全根除。
結論
的同時發現預期結果和額外的刪除APCGene代表了全基因組測試揭示的二次發現的健康和倫理管理的相關問題的一個例子。此外,本報告強調有必要為患有糖尿病的兒童製定專門的監測指南APC相關息肉,提出了是否懷疑和篩查的問題APC散發型肝母細胞瘤的相關情況。
背景
目前,染色體微陣列(CMA)是用於智力障礙(ID)和/或多種來源不明的先天性異常患者的第一級基因檢測手段,檢測DNA拷貝數變異(CNVs),即微重複或微缺失[1].
在致病性CNVs中,22q11.2缺失綜合征(22q11.2 ds) (OMIM #192430)是最常見的微缺失障礙之一,其發病率相對較高,估計約為1:4000新生兒,可能由於臨床錯誤/認識不足而被低估。主要臨床表現包括麵部畸形、先天性心髒缺陷、伴有或不伴有齶裂的齶咽功能不全、胸腺發育不全/發育不全、免疫缺陷和/或自身免疫障礙、甲狀旁腺發育不全、發育遲緩(通常是邊緣性智力功能)、學習障礙、精神障礙、腎髒、眼部和骨骼畸形、聽力損失和喉部異常[2].最常見的雜合子微缺失,導致DiGeorge/速心麵綜合征,包括∼3 Mb,而8-10%的個體表現出∼1.5 Mb嵌套缺失,導致相似但總體溫和的表型[3.].在90%的病例中,該缺失是偶發的,由從頭雜合子缺失引起,而在其餘10%的個體中,該缺失以常染色體顯性模式從偶爾表現出輕微症狀的父母那裏遺傳而來[2].
22q12 . 2ds可以使用FISH測試(熒光原位雜交)與特定探針定位該區域,或使用全基因組方法,如CMA進行診斷。第一種方法可能對臨床懷疑程度較高的患者有益,但它可能誤診非典型嵌套缺失患者[2].CMA可能對臨床表現不明顯的患者和/或經驗不足的衛生專業人員更直接;然而,作為全基因組分析,它可以揭示偶然的微缺失/微複製,可能與患者相關,必須正確地溝通和管理。
在這裏,我們報告了一個臨床懷疑為22q12 .2 ds的兒童,其診斷過程導致了一個偶然的遺傳發現,對臨床管理和預後有重要的影響。
案例展示
男性先證者是南美血統的非血緣健康父母的第二個孩子。家族史與此無關。妊娠平安無事,足月出生的嬰兒體重2600克(第10百分位),長48厘米(第25百分位),枕額圍32厘米(第10百分位),Apgar評分9/10。臍部疝很明顯。他的生長在6個月大之前是正常的,但在6個月大的時候出現了漸進式的放緩。他的父母報告說他經常上呼吸道感染,並接受抗生素治療。
19個月大時因腸胃炎住院期間,他接受了神經學檢查,結果顯示精神運動發展遲緩(他隻會說一個詞,也不會獨自行走)、張力不足、過度嗜睡和社交能力差。腦及腦幹磁共振成像(MRI)顯示腦室係統輕度畸形,海馬不對稱且略垂直,腦橋前後徑輕度縮小。心髒和內分泌檢查正常。血常規檢查顯示為缺鐵引起的微細胞性貧血,輕度低白蛋白血症和低鈣血症。當孩子21個月大時,在第二次因皰疹性口炎住院康複期間,耳鼻喉科醫生對夜間打鼾進行了評估,並建議扁桃體切除術。
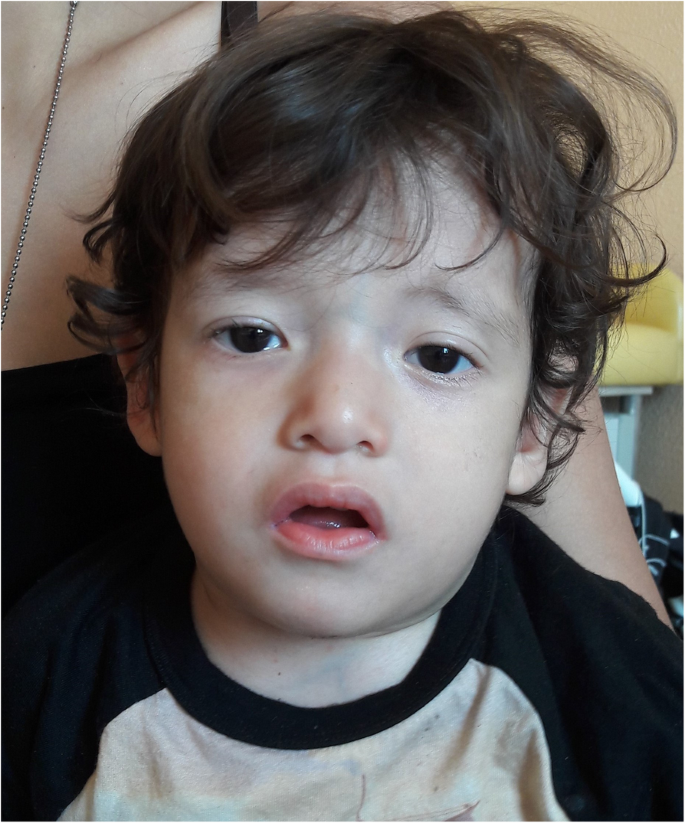
對於輕微的精神運動遲緩,發育不良和大腦異常,他被轉給了遺傳顧問。在他的第一次基因評估中,他的體重是9.5公斤(<第三百分位),他的頭圍是46厘米(<第三百分位)。觀察到輕度提示22q12 . 2ds的麵部異常,包括雙顳部收縮、低置耳、稀疏眉毛、短瞼裂、雙側內眥皺襞、鼻梁凹陷、管狀鼻和輕度鼻翼發育不良(圖2)。1).
由於病史和麵部外觀,對患者及其父母進行了CMA分析。采用60聚寡核苷酸探針技術(SurePrint G3 Human CGH 8x60K, Agilent Technologies, Santa Clara, CA, USA)對從外周血中提取的DNA進行CMA分析。根據製造商的協議(Agilent olignucletide Array-Based CGH for Genomic DNA Analysis, 7.5版本)對DNA樣本進行標記、純化和雜交。使用Agilent Feature Extraction生成原始數據,並使用ADM-2算法(Agilent Technologies, Santa Clara, CA)對CytoGenomics 4.0.3.12進行分析。為了提高結果的準確性,采用了二倍體峰集中算法。
將像差濾波器設置為最小3個連續探測個數/區域,最小絕對平均對數比(MAALR)為±0,25。第二次分析的MAALR為±0,15,每個區域最少使用3個探針來檢測低水平鑲嵌。
拷貝數變異如果與基因組變異數據庫(http://projects.tcag.ca/variation/).基因組坐標符合人類基因組參考聯盟(GRch37/hg19)的37構建(2009年3月)。
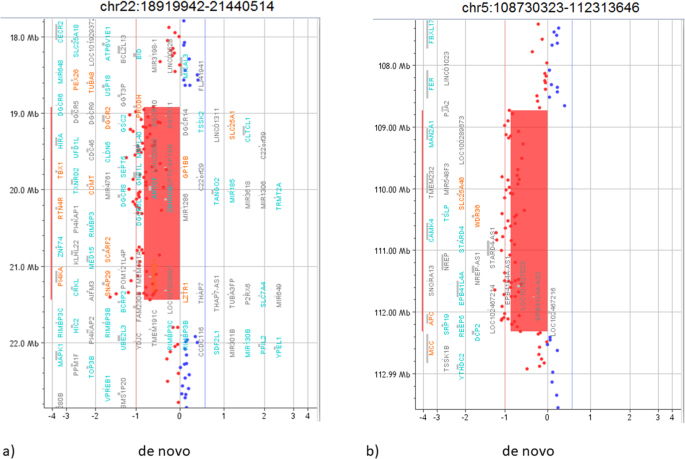
分析發現了四次重排1):兩個微重複的小尺寸,它們的基因含量和親本來源提示可能是良性作用。一例從頭重排是與22q11.2缺失綜合征相關的典型22q11.21微缺失(圖1)。2a).此外,發現了一個全新的5q21.3q22.2微缺失:這個3.6 Mb的缺失涉及12個OMIM基因,包括APC描述…狀況的APC相關的息肉病(無花果。2b)。
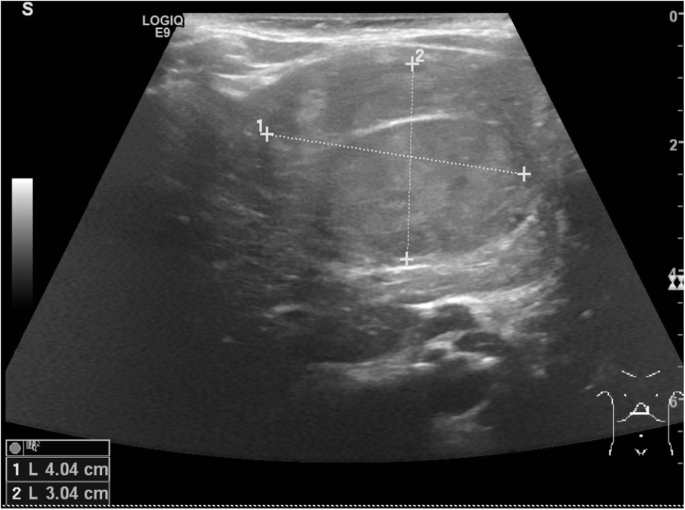
由於基因測試的結果,先證者被登記參加量身定製的隨訪。第一次檢查時,檢測到異常高的α胎蛋白(αFP)水平(266.4 μg/L,正常範圍< 7 μg/L),腹部超聲顯示肝左葉有一個4 × 3 cm的實性腫塊,邊緣清晰,呈橢圓形和雙葉狀(圖)。3.).為了對病變進行更準確的評估,進行了腹部磁共振(MRI)檢查,確認了肝髒腫塊的存在,位於II-III-IV段。T2加權圖像呈不規則高信號,T1呈低信號,多結節結構,有定界假包膜,T2和T1序列均呈低信號。靜脈內順磁性造影劑不規則強化,靜脈期增強,晚期持續高密度條紋。根據強化、結構和血管關係的不規則形態,該病變與肝母細胞瘤(HB)的診斷一致。
該患者隨後被轉診到國立腫瘤研究所的兒科腫瘤科。臨床檢查無明顯差異。血液檢查證實αFP水平升高(97.5 μg/L);β人絨毛膜促性腺激素(βhCG)值正常。胸部x光檢查正常,無任何胸部病變。考慮到這些評估,我們對腫塊進行了核心針活檢,並作出了胎兒上皮性肝母細胞瘤的診斷。
在此診斷後,根據目前極低風險肝母細胞瘤患者的指南進行治療。首先進行左肝葉切除術(切除II-III節段),無任何術後並發症。組織學檢查證實了診斷和手術的激進性(胎兒上皮性肝母細胞瘤;有絲分裂指數> 2/10高功率場(HPF);患腫瘤切除的利潤)。在此之後,考慮到組織學證據,2個周期的順鉑(100 mg/m)輔助化療2連續靜脈滴注48h),從術後1個月開始,間隔21天給藥。在治療過程中,αFP值逐漸下降,在化療結束2個月後恢複正常。除第一輪化療後出現上呼吸道感染外,該治療未出現血液係統或其他毒副反應,可能與22q12 . 2ds測定的易感性有關。
治療結束18個月後,患兒無腫瘤複發跡象。他繼續進行定期的特異性腫瘤隨訪,包括臨床評估、放射學評估(腹部超聲檢查)和血清αFP劑量;此外,他被轉介到遺傳性胃腸道癌綜合征的專家進行適當的FAP監測。他還通過血液學檢查、眼部檢查和甲狀腺超聲繼續進行遺傳隨訪。在最新的評估中,甲狀腺功能參數被改變:他被轉到內分泌科醫生進行適當的診斷框架和治療。
討論和結論
陣列- cgh分析證實了22q12 . 2ds的臨床懷疑,並導致由於刪除的偶然發現癌症易感性綜合征APC基因。
種係單倍不足APC家族性腺瘤性息肉病(FAP)是一種高度滲透的疾病,其特征是發展為各種直腸和結腸腺瘤和早發性結直腸癌[4].大多數致病的變異APC基因是喪失功能的單核苷酸變異[5];大的細胞遺傳學缺失,包含APC基因,很少有報道,估計占2-3%的患者[6,7].的APC基因種係突變和缺失不僅與結直腸腫瘤發生有關,還與其他各種癌前病變和惡性病變有關:十二指腸、空腸和胃息肉、甲狀腺乳頭狀癌、硬纖維瘤和胚胎腫瘤,如肝母細胞瘤(HB)和成髓母細胞瘤。整個APC基因缺失似乎主要導致典型的FAP表型,有成千上萬的腺瘤性結腸息肉和腸外FAP相關表現,如上消化道息肉、先天性視網膜色素上皮肥大(CHRPE)和硬纖維瘤[6,8,9].
我們先證者中發現的22q11.2微缺失可以解釋精神運動發育遲緩、張力減退、社交障礙、傳染病頻繁發作、腦電圖和腦MRI異常、低鈣和甲狀腺功能減退以及特征性麵部畸形的臨床特征。盡管22q12 . 2ds尚未明確與惡性腫瘤風險增加相關,但在這些患者中很少有兒童癌症病例的報道[10,11,12:特別是斯卡通等人。[10和McDonald-McGinn等人。[12]分別描述了1例和2例22q12 . 2ds合並肝母細胞瘤。獨特的免疫缺陷易導致更高的感染性疾病發生率,也易引起致癌病毒和腫瘤監測功能受損,以及參與致癌物質解毒的某些特定基因(如兒茶酚- o -甲基轉移酶基因)的雜合缺失,都可能是複雜致癌過程中的並發原因[11].
在這個場景中,22q12 . 2ds可能對HB的開發以及APC缺失仍然是我們病人的主要誘因。事實上,攜帶基因突變或缺失的患者發生HB的風險增加APC估計確實很低,介於0.3至1.6%之間[13],但約為普通人群(0.0001%)的750-7500倍[14].FAP兒童確診HB的中位年齡與散發性兒童相似,主要在6個月至3歲之間[15].由於HB的預後嚴格依賴於早期發現,因此,完全切除,篩查試驗患者的種係單倍體功能不全APC是強製性的。除了提高生存率之外,它還可以降低治療強度,減少器官毒性。到目前為止,還沒有一個關於監視時間和方法的標準協議。考慮到估計的風險,與其他遺傳易感條件(如Beckwith-Wiedemann綜合征)類似,一些研究建議至少每3個月結合肝超聲監測αFP水平[16],直到7歲[13,14,15,16,17].
這份報告和以前的報告也提出了是否要懷疑和篩選的問題APC散發型肝母細胞瘤的相關情況。HB約占所有兒科腫瘤的1%,是兒童最常見的肝癌:如果我們的病例之前沒有檢測,他的HB會被歸為“散發”型,因為他沒有明顯的FAP家族史或其他表現。異常激活Wnt-信號通路在絕大多數HBs中通過-連環蛋白基因的體細胞突變發生(CTNNB1, OMIM *116806),特別是涉及外顯子3的點突變或幀內缺失[16,17,18];APC蛋白是一種重要的負調控蛋白Wnt信號通路。報告的種係率APC明顯散發的HBs的突變是高度可變的:Sumazin等。[18]發現約有1.1%的散發型HBs伴APC種係突變,而Aretz等人[15和楊等人。[19]報告的發生率為10-20%,因此提示為常規APC對所有HB患者進行檢測。自體細胞CTNNB1和生殖係APC突變已被證明在肝母細胞瘤和迄今研究的所有腫瘤類型中以相互排斥的方式發生[18,19,20.],體細胞激活的鑒定CTNNB1HB患者的突變直接降低了攜帶種係的風險APC突變(20.].基於這些數據,兩步方法將是可取的:檢測的體細胞突變CTNNB1首先應對腫瘤塊進行免疫化學和/或遺傳分析;那麼所有CTNNB1陰性患者應進行種係篩查APC結合測序方法和MLPA(多重連接依賴探針擴增)檢測突變/缺失。對於有肝外FAP表現或有提示家族史的病例,這必須是第一級分析。
就像APC眾所周知,許多其他基因和相關綜合征在兒童年齡患癌症的風險增加;其中至少8-10%的癌症易感性基因有種係突變APC作為這類患者中第二常見的突變基因[21].對明顯散發的兒童癌症進行基因分析的詳細指導方針缺失:檢測所有兒童癌症患者的種係癌症易感性基因可能是一種資源的浪費,最重要的是可能導致大量未知的顯著變異,並由此帶來這些類型的“不確定診斷”帶來的巨大家庭影響。相反,作為第一步,體細胞腫瘤篩查不僅可以提供不同分子風險亞型的信息並幫助臨床管理,還可以幫助區分散發腫瘤與遺傳易感性綜合征相關的腫瘤。
我們的病例是基因“雙重診斷”的一個完美的例子,通過基因組檢測如CMA:如果我們要確認臨床懷疑22q12 . 2ds使用FISH技術,我們將錯過APC刪除對病人的治療有重要影響。如今,全基因組檢測,如CMA和全外顯子組測序(WES),不僅大大提高了診斷率,而且也提高了意外和不確定發現的比率。談到CMA,偶然發現可以定義為意外的cnv,與患者的臨床指征沒有直接關係,但有一些醫學意義,賦予癌症的易感性,神經退行性成人發病病理或揭示攜帶者狀態。這些偶然發現也與對其他家庭成員的影響有關,往往導致對看似健康的個人進行關鍵檢測,並引發具有象征意義的倫理困境,如對童年時期的兄弟姐妹進行檢測[22].而對於外顯子組和基因組測序,是否以及哪些偶然變異必須報告是一個持續討論的話題[23], CNVs的貢獻尚未得到充分的研究,特別是考慮到它目前被用作第一診斷工具。一些大型研究調查了偶然cnv的比例及其遺傳谘詢意義[24,25,26,27].特別是,根據Talukdar等人的文獻薈萃分析,在接受CMA的個體中,涉及癌症易感基因(CSGs)的CNVs發生率為0.6% [17].根據這個英國共識小組,微刪除包括APC被歸類為“涉及一種癌症易感基因的可識別的缺失/複製綜合征,其終生癌症風險可從文獻中證明明顯升高,因此建議進行監測”,因此必須提交實驗室報告[17].在意大利的背景下,缺乏關於這一專題的具體建議;然而,我們堅決認為,在試驗前谘詢中,醫學遺傳學家必須以一份適當的同意書將可能的偶然發現告知患者或其父母,他們可以自由決定是否知道。然而,如果對於沒有治療或預防性護理的成人發病疾病,患者不知情的意誌更容易被接受,那麼發現偶然的cnv可能導致治療/預防措施,特別是對兒童,就為臨床醫生帶來了一個嚴重的倫理問題[27].就我們的案子來說,不上報APC刪除會造成道德上的困難,並對病人的健康造成擔憂;這讓我們意識到,對於附帶cnv的報告,國際準則是多麼的必要。
總之,該報告顯示了一個22q12 . 2ds兒童,在APCCMA的發現。這一偶然發現涉及到一種癌症易感狀態,讓我們向家人披露了它,導致了肝母細胞瘤的早期診斷和完全根除。這個案例突出了當前全基因組檢測和偶然發現的一些新出現的健康管理和倫理問題,甚至更值得注意的是這些分析也可用於非遺傳醫療保健專業人員。在這種情況下,參與臨床管理的不同醫療保健專業人員之間的緊密合作顯得至關重要。
數據和材料的可用性
數據共享不適用於本文,因為在當前研究期間沒有生成或分析數據集。
改變曆史
2021年9月14日
縮寫
- 22 q11.2ds:
-
22 q11.2缺失綜合症
- α外交政策:
-
甲胎蛋白
- β線:
-
β人絨毛膜促性腺激素
- CMA:
-
染色體微陣列
- 基因拷貝數異變:
-
人類基因組變異
- csg:
-
癌症易感基因
- FAP:
-
家族性腺瘤息肉病
- 魚:
-
熒光原位雜交
- 高通濾波器:
-
高功率領域
- HB:
-
肝母細胞癌
- ID:
-
智力障礙
- MAALR:
-
最小絕對平均對數比
- 核磁共振成像:
-
磁共振成像
- 離岸金融中心:
-
Occipitofrontal周長
- 韋斯:
-
全外顯子組測序
參考文獻
Miller DT, Adam MP, Aradhya S, Biesecker LG, Brothman AR, Carter NP,等。共識聲明:染色體微陣列是對發育障礙或先天性異常個體的一級臨床診斷測試。中華醫學雜誌。2010;86:749-64。
McDonald-McGinn DM, Emanuel BS, Zackai EH等。22q11.2刪除綜合征。1999年9月23日[更新2020年2月27日]。作者:Adam MP, Ardinger HH, Pagon RA等人,編輯。GeneReviews®。西雅圖:華盛頓大學,西雅圖;1993 - 2020。
Burnside RD. 22q11.21缺失綜合征:近端、中央和遠端缺失及其相關特征的綜述。Cytogenet Genome Res. 2015;146(2): 89-99。
Kerr SE, Thomas CB, Thibodeau SN, Ferber MJ, Halling KC.評估家族性腺瘤性息肉病個體的APC種係突變:梅奧診所1591次連續試驗的經驗回顧。中華醫學雜誌2013;15:31-43。
Hirschman BA, Pollock BH, Tomlinson GE。家族性腺瘤性息肉病患兒肝母細胞瘤APC突變譜。J Pediatr。2005;147:263-6。
阿瑞茲·斯泰寧·D, Uhlhaas·S, Pagenstecher C, Mangold E, Caspari R,等。大量亞顯微基因組APC缺失是典型家族性腺瘤性息肉病的常見原因。中華醫學與流行病學雜誌2005;42(2):185-92。
Wachsmannova L, Mego M, steurkova V, Zajac V, Ciernikova S. APC基因綜合突變篩選的新策略。贅生物。2017;64(3):338 - 43。
Quadri M, Vetro A, Gismondi V, Marabelli M, Bertario L,等。家族性腺瘤性息肉病APC重排:缺失長度和斷點序列的異質性奠定了相似的表型基礎。家族性癌症。2015;14:41-9。
Michils G, Tejpar S, Thoelen R, van Cutsem E, Vermeesch JR, Fryns J-P,等。15%突變陰性的典型息肉病(FAP)患者存在APC基因的大量缺失:一項比利時的研究。哼Mutat。2005;25(2):125 - 34。
斯卡通A, Caruso G, Marzullo A, Piscitelli D, Gentile M, Bonadonna L,等。腫瘤疾病和缺失22q11.2:兩例多中心研究和報告。兒科病理分子醫學2003;22:323-41。
Stevens T, van der Werff ten Bosch J, De Rademaeker M, van Den Bogaert A, van Den Akker M. 22q11.2缺失綜合征的惡性風險。臨床病例報告2017;5:48 - 90。
McDonald-McGinn DM, Reilly A, Wallgren-Pettersson C, Hoyme HE, Yang SP, Adam MP,等。22q11.2染色體缺失綜合征(digegeorge綜合征/心麵速度綜合征)中的惡性腫瘤。中華醫學雜誌。2006;40(8):926 - 926。
Achatz MI, Porter CC, Brugières L, Druker H, Frebourg T, Foulkes WD,等。兒童遺傳性胃腸道癌綜合征的癌症篩查建議及臨床處理。《臨床癌症雜誌》2017;23:e107-14。
Krawczuk-Rybak M, Jakubiuk-Tomaszuk A, Skiba E, Plawski A. APC基因突變導致的肝母細胞瘤。兒科胃腸病學雜誌2012;55:33 - 6。
阿瑞茲S,科赫A,烏爾哈斯S,弗裏德爾W,普羅普P,馮·施維尼茨D,等。有家族性腺瘤性息肉病風險的兒童是否應該進行肝母細胞瘤篩查?有明顯散發性肝母細胞瘤的兒童是否應該進行APC種係突變篩查?兒科血癌。2006;47:811-8。
李鵬飛,李誌強,李誌強,李誌強。經分子證實的家族性腺瘤性息肉病患者的肝母細胞瘤:臨床特征和監測篩選的基本原理。兒童血癌。2018;65:e27103。
Talukdar S, Hawkes L, Hanson H, Kulkarni A, Brady AF, Mcmullan DJ,等。具有次生影響的結構畸變(SASIs):在拷貝數變異(CNVs)分析中發現的癌症易感基因報告的一致建議。中華醫學雜誌2019;56:718-26。
蘇馬津P,陳勇,Treviño LR, Sarabia SF, Hampton OA, Patel K,等。肝母細胞瘤的基因組分析確定了不同的分子亞群和預後亞群。肝髒病學。2017;65(1):104 - 21所示。
楊A, Sisson R, Gupta A, Tiao G, Geller JI。肝母細胞瘤的種係APC突變。兒童血癌。2018;65:e26892。
杜賓克·許傑,霍林克·IHIM, Avenca Valente C,等。基於組織的新型ß-catenin基因和免疫組化分析排除肝母細胞瘤兒童家族性腺瘤性息肉病。兒童血癌。2018;65:e26991。
張傑,Walsh MF,吳剛,Edmonson MN, Gruber TA, Easton J,等。兒童癌症易感性基因的種係突變。中華醫學雜誌2015;373:2336-46。
Brodeur GM, Nichols KE, Plon SE, Schiffman JD, Malkin D.兒童癌症易感性和監測:概述,致敬Alfred G. Knudson Jr. clinin Cancer Res. 2017;23: e1-5。
Green RC, Berg JS, Grody WW, Kalia SS, Korf BR, Martin CL,等。ACMG關於報告臨床外顯子組和基因組測序偶然發現的建議。地中海麝貓。2013;15(7):565 - 74。
Pichert G, Mohammed SN, Ahn JW, Ogilvie CM, Izatt L.陣列比較基因組雜交檢測癌症易感性基因的意外發現:問題是什麼?中華醫學與流行病學雜誌2011;48(8):535-9。
Boone PM, Soens ZT, Campbell IM, Stankiewicz P,張SW, Patel A,等。在臨床人群中通過常規基因組檢測發現的偶然拷貝數變異。麝貓醫學。2013;15(1):45 - 54。
Hamm JA, Mikhail FM, Hollenbeck D, Farmer M, Robin NH。通過陣列比較基因組雜交偶然檢測癌症易感性基因拷貝數變化。中華兒科雜誌2014;165(5):1057-9 e1-4。
Lefebvre M, Sanlaville D, Marle N, Thauvin-Robinet C, Gautier E, Chehadeh SE,等。基因谘詢的困難和基因陣列cgh偶然發現的倫理意義:一項7年的全國性調查。麝貓。2016;89(5):630 - 5。
確認
這項工作由歐洲罕見先天性畸形和罕見智力殘疾參考網絡(ERN-ITHACA)完成。
資金
沒有資金。
作者信息
作者和聯係
貢獻
DM對患者進行評估,協調診斷和隨訪過程,並負責研究的構思和設計。急診室收集了這些信息並起草了最初的手稿。BR和DM對手稿進行了嚴格的審閱和修改。RS和SG進行了染色體微陣列分析、數據解釋和方法起草。LB, GG和SS提供了患者的腫瘤治療,並幫助起草了手稿。AC進行腹部超聲。PGM嚴格地修改了手稿並監督病人的管理。所有作者閱讀並批準了最終稿件。
相應的作者
道德聲明
倫理批準和同意參與
已獲得家長的知情同意。
同意出版
本病例報告及相關圖片的發布已獲得患者法定監護人的書麵知情同意。
相互競爭的利益
作者聲明他們沒有競爭利益。
額外的信息
出版商的注意
beplay外围下载施普林格自然對出版的地圖和機構附屬的管轄權要求保持中立。
權利和權限
開放獲取本文遵循創作共用署名4.0國際許可協議(Creative Commons Attribution 4.0 International License),該協議允許在任何媒體或格式中使用、分享、改編、分發和複製,隻要您給予原作者和來源適當的署名,提供創作共用許可協議的鏈接,並說明是否有更改。本文中的圖片或其他第三方材料包含在文章的創作共用許可中,除非在材料的信用額度中另有說明。如果材料不包含在文章的創作共用許可中,並且您的預期用途不被法律法規允許或超出了允許的用途,您將需要直接從版權所有者那裏獲得許可。欲查看此許可證的副本,請訪問http://creativecommons.org/licenses/by/4.0/.創作共用公共領域奉獻放棄書(http://creativecommons.org/publicdomain/zero/1.0/)適用於本文提供的數據,除非在數據的信用額度中另有說明。
關於這篇文章
引用這篇文章
羅西娜,E.,裏納爾迪,B.,西利皮尼,R.。et al。偶然發現兒童APC缺失:雙重麻煩還是雙重機會?-一份病例報告。斜體字J Pediatr4731(2021)。https://doi.org/10.1186/s13052-021-00969-x
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-021-00969-x
關鍵字
- 22 q11.2缺失綜合症
- APC
- 肝母細胞癌
- DNA微陣列
- 偶然的發現
- 病例報告