摘要
背景
先天性高胰島素症通常發生在新生兒低血糖,但甚至可以出現在兒童或青少年不同類型的糖代謝紊亂。目前的診斷算法沒有考慮到晚期發病的情況。
患者和方法
本文描述了在那不勒斯費德裏科二世大學診斷的22名受試者的臨床和實驗室數據:根據分子缺陷將患者分為通道缺陷、代謝缺陷和未識別的分子缺陷。特別關注的是三個遲交的案例。
結果和結論
早期的診斷算法可能無法識別晚期病例。因此,從發病年齡開始設計一個新的流程圖似乎是合適的,同時考慮到晚期發病病例可以顯示糖代謝紊亂,而不是糖尿病、葡萄糖不耐受、餐後低血糖和妊娠期糖尿病等低血糖危機。
背景
先天性高胰島素症(CH),最早由Stanley定義[1],代表嬰兒期持續低血糖症(HY)最常見的病因,估計在一般人群中發病率為1:40.000-50.000,在近親情況下,發病率可達1:2500 [2].迄今為止,它在意大利的流行情況並不為人所知[3.,4].CH是由於β -細胞膜通道或細胞內代謝途徑的改變,涉及胰島素分泌。特別是,由K-ATP通道突變引起的通道缺陷(ChD)約占所有CH病例的36% [5)和影響ABCC8而且KCJN11它們分別編碼磺酰脲受體1 (SUR1)和Kir6.2 (K-ATP通道亞基)。代謝缺陷(MeD)是由β -細胞胞內信號傳導缺陷引起的。迄今為止,已知有12個基因與MeD病例有關[5,6];GCK和GLUD1是較少涉及的基因。如果新生兒出現持續性HY,且血液胰島素水平不適當,則懷疑為CH。進一步的診斷標準可以是靜脈葡萄糖需要量大於8 mg/kg/min [7,8].Maiorana等人的流程圖[9建議從代謝篩查開始,並指出18所有病例均應進行F-DOPA PET檢查。
眾所周知,CH的診斷也可發生在青少年和報告有除HY以外症狀的成人,如輕度高血糖和妊娠期糖尿病[10,11,12,13,14],從而證明晚期診斷為慢性阻塞性肺病是合理的[15].
根據我們的臨床經驗,我們提出了一個新的流程圖,它代表了其他文獻中已經提出的診斷範圍的擴展,其優點是使診斷更快、更準確。
患者和方法
我們的研究報告了22名在那不勒斯費德裏科二世大學兒科糖尿病區域中心接受CH診斷並隨訪至少3年的患者。
CH的診斷是基於在新生兒/嬰兒期開始的低血糖危機期間檢測可測量的胰島素水平。按照現行新生兒病例診斷流程圖進行分子診斷;一個準確的臨床調查是必不可少的診斷三個晚期病例。
根據他們的遺傳缺陷,患者被分為三組:ChD, MeD和不明分子缺陷。
收集的數據包括:家庭中的HY和其他糖代謝紊亂(GMD),出生體重大(LGA)和足月或早產,出生72小時前後發生HY,對二氮氧(Dx)的反應,手術治療,以及在隨訪中存在糖尿病、肥胖和神經損傷。冠心病患者的資料(ABCC8-mutation)已在表中報道1表中MeD數據和未確認缺陷2.
結果
在所有22例患者中,有16例接受了分子診斷:12例ABCC8變異(54%),2GLUD1(9%), 1GCK(4%)和1HADH(4%)。因此,在這一人群中,基因缺陷的檢出率為73%,高於Rahman等人報道的45-55% [5].
在7/12的冠心病家庭中發現GMD,在2/4的MeD家庭中發現GMDGLUD1突變)和3/6的未確認缺陷;在6/12的冠心病病例中發現早產,其他類別均未發現早產;在6/12的冠心病病例中檢測到LGA,而在1例MeD中僅檢測到LGAGCK突變);11/12的冠心病和3/6的不明缺陷在出生後72小時內出現HY;在6/12冠心病患者和所有MeD +未確認缺陷受試者中發現Dx響應性;隨訪發現4/12冠心病患者中有糖尿病(2例接受了胰腺切除術,2例晚期就診);MeD和未確認的缺陷均無;在隨訪中,5/12冠心病患者、1/4 MeD患者和3/6未確定缺陷患者中發現肥胖;隨訪發現4/12 ChD(受試者5號癲癇,受試者7號癲癇和嚴重發育遲緩,受試者9號和10號發育遲緩),1/4 MeD(這是G. V,下文詳細描述)和1/4未確定的缺陷(癲癇)。
我們已經執行18F-DOPA PET-CT在14/22例患者中均可見擴散型。由於缺乏3年隨訪,1例經手術(部分胰腺切除術)解決灶型的新生兒和另外4例病例未納入本研究。
過期提交情況
B. B.A.家族(男性,12歲)因偶爾檢測到無症狀的空腹高血糖而被轉給我們。他出生時早產(35周)和LGA (4150 g),妊娠以GDM為特征。B.A.和他的兄弟B. B., 17歲,在新生兒和兒童期出現了餐後HY;3年後,B.B.也被診斷為糖尿病。他們的母親、外祖母和姑母均有糖尿病,並接受了二甲雙胍治療。母親首次妊娠以GDM為特征,在LGA新生兒中遲疑。排除自身免疫性糖尿病後,b.a最初采用低血糖指數飲食治療,後來采用磺酰脲類治療。雜合突變c.G4435 > A (p.Gly1479Arg)(已在文獻中報道為該表型變異性的原因)[12在b.a.、B.B.及其母親中檢測到];祖母和阿姨拒絕進行基因調查。b.b.b的數據見表1(1號和2號病人)。
G.V.(女,15歲)因偶檢出HY而被介紹給我們。她足月出生(40周),LGA(4800克),2歲時被收養;新生兒神經損傷的原因不明。在兒童時期,她表現為廣泛性癲癇,用丙戊酸治療,中度精神運動障礙。在HY(葡萄糖值42 mg/dL)期間進行的實驗室調查顯示,高胰島素血症(20,1 μUI/ml),而銨、乳酸、皮質醇、IGF-1、血漿氨基酸、酰基肉堿和尿有機酸水平正常。葡萄糖激酶基因V455L雜合突變(GCK)檢測;這種突變在文獻中尚未有描述。她開始以8 mg/kg/死亡劑量的dx治療,反應良好。G.V.數據見表21號(病人)。
流程圖
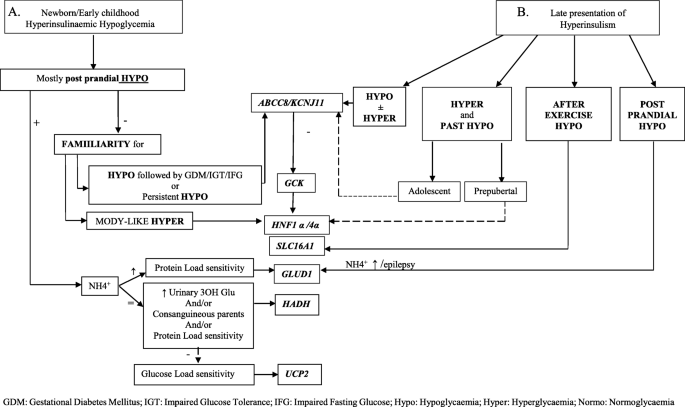
從對報告病例的觀察,特別是考慮到晚期病例,我們試圖設計一個新的CH診斷流程圖(圖。1)擴展了Maiorana算法的診斷部分,第一步加上了出現的年齡:A節指的是早熟出現的CH病例,B節指的是出現較晚的CH病例。在A節中,餐後HY的發生指向GLUD1,HADH或UCP2[16,17,18,19]缺陷,這取決於相關的代謝結果。有HY陽性家族史的非特異性低血糖模式可以指向ABCC8 / KCJN11突變;如果他們沒有改變,首先GCK然後HNF1α/ 4α應該進行測試,正如已經報道的那樣。在B段,低血糖/高血糖波動的非特異性低血糖模式指向ABCC8 / KCJN11突變:如果沒有改變,首先GCK然後HNF1α/ 4α應該被測試。輕度高血糖和既往HY病史指向ABCC8 / KCNJ11或HNF1α/ 4α突變,特別是在晚發病例中。發生在體育鍛煉後的HYSCL16A1突變(20.,21];餐後HY,特別是與癲癇或高氨血症相關的,可提示GLUD1突變(16,17].
討論
根據文獻對22例患者的觀察結果是:冠心病患者在前72 h內常見GMD、LGA、早產和早熟的發生率較高;MeD和未確定缺陷具有良好的dx響應性,但冠心病隻有部分響應性[22].
有關CH病例隨訪的文獻通常隻關注手術後繼發的糖尿病:在我們的病例中,兩名受試者在次全胰腺切除術後出現糖尿病,另外兩名是b家族的兩個兄弟,他們有ABCC8突變。有趣的是,9/22名患者在隨訪中出現肥胖:5名患者有冠心病,1名患者有GLUD1, 3名患者有未確定的缺陷。這一發現可能與ABCC8在肥胖易感性中的作用有關,正如已經在2型糖尿病患者中報道的那樣[23],可能是高胰島素症導致的;然而,據了解,有些ABCC8單核苷酸多態性似乎可以預防代謝綜合征[24].此外,在4名受早熟和嚴重形式冠心病影響的受試者中,1名患有GCK(上文所述的G.V.病例),1名患有未確定缺陷的患者中,神經功能障礙的存在與文獻一致。
CH診斷算法從代謝研究開始[16,17,25,26]並進行分子診斷和基因型-表型相關性。Dx試驗被認為是CH治療的關鍵步驟:耐藥患者必須使用奧曲肽治療,並需要特征18F-DOPA PET-CT,以解決適當的手術(彌漫性形式的近全胰腺切除術或局灶型的局限性切除)[2,6].另一方麵,最近的方法是從特殊代謝發現的研究開始指導遺傳篩查,這是選擇患者的基本步驟,而不是dx反應性18F-DOPA磁共振(9].事實上,這些作者已經發現,雖然罕見,但一些病灶形式可能是dx響應的,可以通過手術完全解決。因此,18F-DOPA PET-CT指的是單隱性父係ABCC8 / KCNJ11當主要致病基因(ABCC8/KCNJ11, HNF1/4, GCK, hah, SLC16A1, UCP2)未發現突變時,尋找非典型形式。
CH可以發生在整個童年或成年時期。所有現有的診斷算法都沒有考慮到晚期表現的病例,這些病例可能代表晚期疾病,也可能是誤診和輕度疾病。眾所周知,ABCC8突變可導致CH,演變為高血糖和妊娠期糖尿病[10,13,27,28].在我們的病例中,B.B.和B.B.家族與之前描述的c.4435G > a突變病例相似[12].
GCK激活突變導致異質表型:症狀的嚴重程度和發病年齡在受影響的個體之間存在顯著差異,即使在同一家族中[22,23].因此,測試GCK在我們的病例中,GCKc.1363G > T突變尚未報道。
我們的經驗表明,更好地診斷CH的算法應該考慮更廣泛的方法,從第一次檢測的年齡開始。當CH發展為糖尿病時,HY通常發生在兒童早期,在隨後的幾年裏,發生在餐後時間,在高血糖指數餐後。如果有HY和/或糖耐量受損、空腹血糖受損或GDM家族史,假設ABCC8 / KCNJ11,HNF1A或HNF4A基因突變是可以表述的。特別是,在ABCC8基因突變,高血糖症一般開始於青春期,而在HNF1α/ 4α在青春期前[10,11,12,13,14].
正如其他人所肯定的,18F-DOPA PET-CT在疑似存在dx無反應性灶型時(盡管一些罕見灶型對二氮氧有反應),如果根本沒有檢測到突變,應進行F-DOPA PET-CT;在這些病人的圖像提供18F-DOPA PET-CT可解決手術治療的選擇[8,9,27,29].因此,在後期演示的情況下,我們可以假設18F-DOPA PET-CT應僅用於排除胰島素瘤,因為它可發生在任何年齡,但在兒童年齡非常罕見,可能代表1型多發性內分泌瘤(MEN1)的表現[30.,31,32].胰島素瘤可以用18F-DOPA PET-CT或(68)Ga-DOTATATE [32].沒有胰島素瘤的嫌疑,很難18F-DOPA PET-CT適用於表現遲發的受試者。ABCC8 / KCNJ11文獻報道的晚期診斷病例大多是由於顯性突變決定了擴散型;同樣,MeD形式都是擴散的[10,11,12,13,14].
在我們的病例中,基因檢測的陽性率為73%(16/22),顯著高於文獻報道的45-50% [5].這可能取決於我們大學醫院糖尿病、代謝和新生兒病理學專家之間的嚴格合作。
結論
總之,由於CH不僅可能開始於新生兒期或嬰兒期,也可能開始於兒童期甚至更晚,因此,通過考慮整個家庭目前和過去的血糖變化,提出一個包括這些病例的診斷流程圖可能是有用的。
數據和材料的可用性
本研究期間產生的所有數據都包含在這篇發表的文章及其補充信息文件中。
縮寫
- CH:
-
先天性高胰島素症
- :為什麼
-
低血糖症
- 冠心病:
-
通道缺陷
- 醫療:
-
代謝缺陷
- SUR1:
-
磺酰脲類受體1
- Dx:
-
氯甲苯噻嗪
- GDM:
-
妊娠期糖尿病
- GMD:
-
葡萄糖代謝紊亂
- 達到:
-
對於孕齡來說很大
參考文獻
嬰兒和兒童的高胰島素血症:診斷和治療。Adv兒感染雜誌1976;23:315-55。
Vora S, Chandran S, Rajadurai VS, Hussain K.嬰兒高胰島素性低血糖:診斷和治療的當前概念。印度Pediatr。2015;52(12):1051 - 9。
法雷特拉F, Athanasakis E, Morgan A, Biarnés X, Fornasier F, Parini R,等。先天性高胰島素血症:一個大型意大利隊列的臨床和分子分析。基因。2013;521(1):160 - 5。
Sogno Valin P, Proverbio MC, Diceglie C, Gessi A, di Candia S, Mariani B,等。意大利嬰幼兒先天性高胰島素症患者的遺傳分析。兒科雜誌2013;79:236-42。
先天性高胰島素血症的分子機製。中國分子內分泌雜誌2015;54(2):R119-29。
先天性高胰島素血症的診斷和治療進展。中華兒科內分泌雜誌2017;9:69-87。
De Leon DD, Stanley CA先天性低血糖障礙:病因學、診斷、治療和結果的新方麵:先天性低血糖障礙研討會的會議記錄,費城,2016年4月。Pediatr糖尿病。2017;18(1):3 - 9。
Roženková K, Güemes M, Shah P, Hussain K.高胰島素血症性低血糖的診斷和治療。中華兒科內分泌雜誌2015;7(2):86-97。
maorana A, Barbetti F, Boiani A, Rufini V, Pizzoferro M, Francalanci P,等。藥物治療治療局灶性先天性高胰島素:基於分子遺傳篩選的診斷算法。性。2014;81(5):679 - 88。
Abdulhadi-Atwan M, Bushman J, Tornovsky-Babaey S, Perry A, Abu-Libdeh A, Glaser B,等。磺酰脲受體1的新突變表現為嬰兒期的高胰島素血症,隨後在青春期早期出現明顯的糖尿病。糖尿病。2008;57(7):1935 - 40。
Vieira TC, Bergamin CS, Gurgel LC, Moisés RS.攜帶失活ABCC8 E1506K突變的家族中高胰島素血症性低血糖演變為妊娠期糖尿病和糖尿病。Pediatr糖尿病。2010;11(7):505 - 8。
Kapoor RR, Flanagan SE, James CT, McKiernan J, Thomas AM, Harmer SC,等。ABCC8/KCNJ11顯性突變導致高胰島素血症低血糖和糖尿病。Diabetologia。2011;54(10):2575 - 83。
Kapoor RR, Locke J, Colclough K, Wales J, Conn JJ, Hattersley AT,等。雜合子HNF4A突變導致年輕人持續高胰島素性低血糖和成熟性糖尿病。糖尿病。2008;57(6):1659 - 63。
Stanescu DE, Hughes N, Kaplan B, Stanley CA, DE León DD.由MODY基因HNF1A和HNF4A突變引起的先天性高胰島素症的新表現。臨床內分泌病學雜誌,2012;97(10):E2026-30。
Delvecchio M, Mozzillo E, Salzano G, Iafusco D, Frontino G, Patera PI,等。意大利兒科內分泌和糖尿病學會(ISPED)糖尿病研究組。2007年至2012年,意大利15個兒科糖尿病中心轉診的病例中,單基因糖尿病占6.3%。中華臨床內分泌雜誌2017;102(6):1826-34。
Kapoor RR, Flanagan SE, Fulton P, Chakrapani A, chdefaux B, Ben-Omran T,等。高胰島素-高氨血症綜合征:GLUD1基因的新突變和基因型-表型相關性中華內分泌雜誌2009;161(5):731 - 531。
Palladino AA, Stanley CA.高胰島素/高氨血症綜合征。中華醫學雜誌2010;11(3):171-8。
Heslegrave AJ, Kapoor RR, Eaton S, chdefaux B, Akcay T, Simsek E,等。3-羥基酰基輔酶a脫氫酶突變功能缺失患者的亮氨酸敏感性高胰島素血症低血糖。《孤兒罕見病》2010;7:25。
ferara CT, Boodhansingh KE, Paradies E, Giuseppe F, Steinkrauss LJ, Topor LS,等。由解偶聯蛋白2顯性突變引起的先天性高胰島素症的新型低血糖表型。中華臨床內分泌雜誌2017;102(3):942-9。
Meissner T, Otonkoski T, Feneberg R, Beinbrech B, Apostolidou S, Sipilä I,等。運動誘發低血糖高胰島素症。兒童科學。2001;84(3):254-7。
Otonkoski T, Kaminen N, Ustinov J, Lapatto R, Meissner T, Mayatepek E,等。體育鍛煉引起的高胰島素性低血糖是一種常染色體顯性特征,其特征是丙酮酸誘導的胰島素釋放異常。糖尿病。2003;52(1):199 - 204。
Pinney SE, MacMullen C, Becker S, Lin YW, Hanna C, Thornton P, Ganguly A, Shyng SL, Stanley CA.與顯性KATP通道突變相關的先天性高胰島素血症的臨床特征和生化機製。中華臨床醫學雜誌。2008;38(6):689 - 689。
Hani EH, Clément K, Velho G, Vionnet N, Hager J, Philippi A,等。法國白種人NIDDM和病態肥胖磺酰脲受體基因位點的遺傳學研究。糖尿病。1997;46(4):688 - 94。
陳玉玲,裴東,洪玉娟,李春春,肖方鋒,吳長忠,林金東,徐春春,張建軍,謝春春。2型糖尿病患者遺傳變異與代謝綜合征嚴重程度的關係。中華分子生物學雜誌;2015;14(1):2518-26。
Arnoux JB, Verkarre V, Saint-Martin C, Montravers F, Brassier A, Valayannopoulos V, Brunelle F, Fournet JC, Robert JJ, Aigrain Y, Bellanné-Chantelot C, de Lonlay P.先天性高胰島素症:診斷和治療的最新趨勢。《孤兒罕見病》2011;6:63。https://doi.org/10.1186/1750-1172-6-63審查。免費PMC文章。
高胰島素血症性低血糖:遺傳機製、診斷和治療。中華醫學雜誌2012;35(4):589-601。https://doi.org/10.1007/s10545-011-9441-2Epub 2012年1月10日審查。PMID: 22231386。
Gutgold A, Gross DJ, Glaser B, Szalat A.診斷一例20歲男性嬰兒先天性ABCC8高胰島素症,評估人為低血糖。中華臨床內分泌雜誌2017;102(2):345-9。https://doi.org/10.1210/jc.2016-3254.
Morishita K, Kyo C, Yonemoto T, Kosugi R, Ogawa T, Inoue T葡萄糖激酶激活突變導致的無症狀先天性高胰島素血症,被視為腎上腺功能不全12年。2017:4709262。https://doi.org/10.1155/2017/4709262Epub 2017 1月9日。
Yorifuji T.先天性高胰島素症:現狀和未來展望。中華兒科內分泌雜誌2014;19(2):57-68。
gemes M, Rahman SA, Kapoor RR, Flanagan S, Houghton JAL, Misra S, Oliver N, Dattani MT, Shah p兒童和青少年高胰島素性低血糖:病理生理學和治療的最新進展。Rev endocmetab Disord. 2020。https://doi.org/10.1007/s11154-020-09548-7.
Jani N, Moser AJ, Khalid A.胰腺內分泌腫瘤。2007;36(2): 431-9 x-xi。審查。PMID: 17533088。
Tuzcu SA, Pekkolay Z, Kılınç F, Tuzcu AK。68Ga-DOTATATE PET/CT可作為胰島素瘤患者的替代成像方法。核醫學技術雜誌2017;45(3):198-200。https://doi.org/10.2967/jnmt.117.192708Epub 2017 8月10日。
確認
不適用。
資金
沒有資金來源。
作者信息
作者和聯係
貢獻
AC和ADM研究數據並撰寫手稿。EM和VF參與了討論並修改了手稿。FMR和PB研究數據。AF構思並修改了手稿。所有作者閱讀並批準了最終稿件。
相應的作者
道德聲明
倫理批準和同意參與
不適用:本文不包含任何作者進行的任何人類參與者或動物研究。
同意出版
受試者和他們的護理人員都書麵知情同意發表他們的病例。
相互競爭的利益
作者聲明他們沒有競爭利益。
額外的信息
出版商的注意
beplay外围下载施普林格自然對出版的地圖和機構附屬的管轄權要求保持中立。
權利和權限
開放獲取本文遵循創作共用署名4.0國際許可協議(Creative Commons Attribution 4.0 International License),該協議允許在任何媒體或格式中使用、分享、改編、分發和複製,隻要您給予原作者和來源適當的署名,提供創作共用許可協議的鏈接,並說明是否有更改。本文中的圖片或其他第三方材料包含在文章的創作共用許可中,除非在材料的信用額度中另有說明。如果材料不包含在文章的創作共用許可中,並且您的預期用途不被法律法規允許或超出了允許的用途,您將需要直接從版權所有者那裏獲得許可。欲查看此許可證的副本,請訪問http://creativecommons.org/licenses/by/4.0/.創作共用公共領域奉獻放棄書(http://creativecommons.org/publicdomain/zero/1.0/)適用於本文提供的數據,除非在數據的信用額度中另有說明。
關於這篇文章
引用這篇文章
A.卡塞塔諾,A.德·馬泰斯,E.莫茲略。et al。先天性高胰島素症的診斷不僅可以發生在嬰兒期,也可以發生在後期:一個來自單一中心經驗的新流程圖。斜體字J Pediatr46歲,131(2020)。https://doi.org/10.1186/s13052-020-00894-5
收到了:
接受:
發表:
DOI:https://doi.org/10.1186/s13052-020-00894-5
關鍵字
- 先天性高胰島素症
- ABCC8
- 低血糖症
- 診斷流程圖